詹森制药有限公司
制造商的细节
目前没有制造商的细节。
分享这个页面
詹森制药有限公司药品
-
Invega Trinza
![Invega Trinza (Paliperidone Palmitate) Injection, Suspension, Extended Release [Janssen Pharmaceuticals, Inc] Invega Trinza (Paliperidone棕榈酸酯)注射,悬挂,延长释放(詹森制药公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=c39e65d7-fa44-4e4c-8b12-a654d3ed0eae&name=invega-27.jpg)
2.1管理指令
INVEGA TRINZA™应每3个月一次。
每个注射必须只能由医疗专业管理。
注射用药物的药物产品应检查视觉对外国政府之前物质和变色。重要的是震动注射器至少15秒,以确保均匀悬浮。5分钟内注入INVEGA TRINZA™剧烈摇晃(见剂量和管理(2.8))。
INVEGA TRINZA™的目的是仅供肌内使用。不执行任何其他路线。避免无意注入血管。管理一个注射的剂量;不管理分为注射的剂量。慢慢注入,深入三角肌和臀肌。
INVEGA TRINZA™必须只使用管理提供的薄壁针在INVEGA TRINZA™包。不要用针从月paliperidone棕榈酸酯延长释放注射悬挂包或其他商业化针来减少堵塞的风险。
三角肌注射
推荐的针头大小管理INVEGA TRINZA™到三角肌是由病人的体重:
对患者体重小于90公斤,1英寸,22计薄壁针建议。重达90公斤以上,患者1½英寸,22日规薄壁针建议。管理的中心三角肌。三角肌注射应该两个三角肌肌肉之间的交替。
臀部注射
不管病人的体重,推荐针大小管理INVEGA TRINZA™的臀部肌肉1½英寸,22计薄壁针。管理upper-outer象限的臀肌。臀部注射应该两臀部肌肉之间的交替。
不完整的管理
为了避免一个不完整的管理INVEGA TRINZA™,确保已经预装好的注射器动摇了至少15秒前5分钟内管理,以确保均匀悬浮,确保针注射期间不得堵塞(见剂量和管理(2.8))。
然而,在一个不完全的服用剂量,不重注剂量剩下的注射器,不管理的另一个剂量INVEGA TRINZA™。密切监控和治疗患者口腔临床上适当补充,直到下一次三个月注射INVEGA TRINZA™。
2.2精神分裂症
成年人
INVEGA TRINZA™之后才使用INVEGA SUSTENNA®(月paliperidone棕榈酸酯延长释放注射悬浮液)已经建立了足够的治疗至少4个月。为了建立一个一致的维持剂量,建议最后两个剂量的INVEGA SUSTENNA®是相同的剂量强度开始前INVEGA TRINZA™。
启动INVEGA TRINZA™当第二个月paliperidone棕榈酸酯剂量计划与INVEGA TRINZA™剂量根据前一个月注射剂量,使用相当于3.5倍高剂量如表1所示。INVEGA TRINZA™可以管理多达7天之前或之后的月度时间点下一个预定月剂量paliperidone棕榈酸酯。
表1。INVEGA TRINZA™剂量为成人患者充分处理INVEGA SUSTENNA®如果最后剂量INVEGA SUSTENNA®是:启动INVEGA TRINZA™在以下剂量:转换从INVEGA SUSTENNA®39毫克剂量没有研究。78毫克273毫克117毫克410毫克156毫克546毫克234毫克819毫克在最初INVEGA后TRINZA™剂量,INVEGA TRINZA™应每3个月接种疫苗。如果需要,调整剂量可以每三个月增加273毫克到819毫克的范围内基于个别病人耐受性和/或有效性。由于长效自然INVEGA TRINZA™,病人的反应调整剂量可能没有明显的几个月(见临床药理学(12.3))。
2.3错过剂量
剂量窗口
失踪的剂量的INVEGA TRINZA™应该避免。如果有必要,病人可以注射2周之前或之后三个月的时间点。
错过了自去年注射剂量3½个月到4个月
如果超过3½月(但小于4个月)运行自上次注射INVEGA TRINZA™,以前管理INVEGA TRINZA™剂量应尽快,然后继续后三个月注射剂量。
错过了自去年注射剂量4个月至9个月
如果4个月,包括9个月的时间,最后注入INVEGA TRINZA™,不管理的下一个剂量INVEGA TRINZA™。相反,使用重启方案如表2所示。
表2。丢失的4个月至9个月后重启方案INVEGA TRINZA™如果最后剂量INVEGA TRINZA™是:管理INVEGA SUSTENNA®,两剂分开一个星期(成三角肌),那么管理INVEGA TRINZA™(成三角肌*或臀部肌肉)1天1天8月后第8天*参见使用三角肌注射针选择基于体重。273毫克78毫克78毫克273毫克410毫克117毫克117毫克410毫克546毫克156毫克156毫克546毫克819毫克156毫克156毫克819毫克错过了自去年注射剂量超过9个月
如果超过9个月的时间,最后注入INVEGA TRINZA™, re-initiate月paliperidone棕榈酸酯治疗延长释放注射悬浮液中描述该产品的处方信息。INVEGA TRINZA™可以恢复病人充分治疗后1年期paliperidone棕榈酸酯延长释放注射暂停至少4个月。
2.4使用利培酮或口服Paliperidone
由于paliperidone利培酮的主要活性代谢产物,应该小心谨慎当INVEGA TRINZA™与利培酮或口头coadministered paliperidone长时间。安全数据涉及伴随使用INVEGA TRINZA™与其他抗精神病药物是有限的。
2.5剂量调整肾损伤
INVEGA TRINZA™尚未系统研究患者的肾功能损害(见临床药理学(12.3))。轻度肾功能障碍患者(肌酐清除率≥50 mL / min < 80毫升/分钟(Cockcroft-Gault公式),调整剂量和稳定病人使用个月paliperidone棕榈酸酯延长释放注射悬浮液,然后过渡到INVEGA TRINZA™(见表1,剂量和管理(2.2)]。(见也使用在特定人群(8.6)和临床药理学(12.3)]
INVEGA TRINZA™不推荐患者中度或重度肾功能损害(肌酐清除率< 50毫升/分钟)(见使用在特定人群(8.6)和临床药理学(12.3)]。
2.6从INVEGA TRINZA™的月Paliperidone棕榈酸酯延长释放注射悬浮液
开关从INVEGA TRINZA™, INVEGA SUSTENNA®(月paliperidone棕榈酸酯延长释放注射悬浮液),1年期paliperidone棕榈酸酯延长释放注射悬挂应该开始3个月后INVEGA TRINZA™剂量,使用低剂量相当于3.5倍,如表3所示。1年期paliperidone棕榈酸酯延长释放注射悬挂应该继续下去,给在每月的间隔。
表3。转换从INVEGA TRINZA™, INVEGA SUSTENNA®如果最后剂量INVEGA TRINZA™是:启动* INVEGA SUSTENNA®3个月后在以下剂量:*中描述的起始剂量的处方信息INVEGA SUSTENNA®不是必需的。273毫克78毫克410毫克117毫克546毫克156毫克819毫克234毫克2.7从INVEGA TRINZA™口服Paliperidone延长释放平板电脑
切换从INVEGA TRINZA™口服paliperidone延长释放平板电脑,每日剂量的paliperidone延长释放平板电脑应该开始3个月后INVEGA TRINZA™剂量和转变未来几个月后最后INVEGA TRINZA™剂量如表4所示。表4提供了剂量转换方案,允许病人之前稳定在不同剂量的INVEGA TRINZA™实现类似paliperidone曝光一次每日paliperidone延长释放平板电脑。
表4。INVEGA TRINZA™和剂量每日一次Paliperidone延长释放转换方案需要获得类似Paliperidone曝光周自去年INVEGA TRINZA™剂量3个月18周超过18周24周超过24周最后INVEGA TRINZA™剂剂量的口服Paliperidone延长释放平板电脑273毫克3毫克3毫克3毫克410毫克3毫克3毫克6毫克546毫克3毫克6毫克9毫克819毫克6毫克9毫克12毫克2.8说明使用
管理每3个月摇注射器至少15秒仅供肌内注射。不执行任何其他路线。
重要的
INVEGA TRINZA™应由医疗专业作为一个单独的注入。不注射剂量划分为多个。
INVEGA TRINZA™的目的是仅供肌内使用。慢慢注入,深入肌肉照顾,以避免注入血管。
在使用前阅读完整的指令。
剂量
本药应每3个月一次。
准备
剥离选项卡标签从注射器和在病人记录。
INVEGA TRINZA™需要更长、更剧烈的震动比INVEGA SUSTENNA®(月paliperidone棕榈酸酯延长释放注射暂停)。剧烈摇动注射器,注射器尖指向上,至少15秒前5分钟内管理(见步骤2)。
薄壁安全针的选择
薄壁安全针是设计用于与INVEGA TRINZA™。因此,重要的是要只使用提供的针头INVEGA TRINZA™工具。
剂量包装内容
肾上腺素注射器薄壁安全针1选择针
针的选择是由注射区和病人的体重。
如果管理三角肌injectionIf病人重:小于90公斤粉红色中心如果管理臀injectionIf病人重:少于90公斤黄色中心90公斤以上黄色90公斤以上黄色的中心枢纽2准备注射
检查悬
摇晃的注射器至少15秒钟后,检查液体在浏览窗口中。
应该会出现暂停制服,乳白色的颜色。
看到小气泡也是正常的。
打开针袋和删除
首先,打开针囊皮封面回一半。在一个干净的表面。
然后,拿着注射器直立,扭曲和橡胶帽删除。
掌握针袋
向后折叠针盖,塑料托盘。然后,牢牢把握针鞘囊,如图所示。
把针
另一只手,拿着注射器的鲁尔接口连接和附加的安全针轻轻顺时针扭转运动。
不删除袋直到注射器和针头安全型依附。
删除针鞘
把针鞘远离针在直线运动。
不要扭曲鞘,因为这可能放松的针注射器。
消除气泡
拿着注射器直立和自来水轻轻做出任何气泡上升到顶部。
仔细去除空气按柱塞杆向上直到一滴液体的针尖端。
3注入
注射剂量
慢慢地注入注射器肌内的全部内容,深入到选定的三角肌或臀部肌肉。
不执行任何其他路线。
注射后4
安全针
注射完成后,用你的拇指或平面安全针的安全装置。针是安全的,当听到“点击”的声音。
正确地处理
处理的注射器和未使用的针在一个批准的专家容器。
-
优塞林Q10抗皱敏感的皮肤
![Eucerin Q10 Anti-wrinkle Sensitive Skin (Octinoxate, Octisalate, Oxybenzone) Lotion [Beiersdorf Inc] 优塞林Q10抗皱敏感肌肤(桂皮酸盐、Octisalate氧苯酮)乳液(Beiersdorf Inc .)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=6868666b-c25e-40d1-9d1f-306bbe9390c1&name=invokamet-05.jpg)
2.1推荐剂量
有个性的起始剂量INVOKAMET (canagliflozin和盐酸二甲双胍)根据病人的当前方案:-在二甲双胍的患者,切换到包含canagliflozin INVOKAMET 50毫克类似的每日总剂量二甲双胍;——在canagliflozin病人,切换到INVOKAMET含有二甲双胍与类似的每日总剂量500毫克canagliflozin;——在患者已经接受canagliflozin和二甲双胍,切换到INVOKAMET包含相同的每日总剂量的每个组件。每天INVOKAMET两次,餐后服用,剂量逐渐升级,减少胃肠道副作用由于二甲双胍(参见剂型和优势(3)]。患者的体积损耗不是以前canagliflozin处理,纠正这种状况之前启动INVOKAMET[见警告和注意事项(5.2),使用在特定的人群(8.5),(8.6),和病人咨询信息(17)]。基于有效性和耐受性而调整剂量不超过二甲双胍的最大推荐剂量2000毫克和300毫克canagliflozin患者60 mL / min / 1.73平方米的表皮生长因子受体或更高版本(见剂量和管理(2.2))。2.2推荐剂量患者肾功能损害
在启动前评估肾功能INVOKAMET并定期。不启动或继续INVOKAMET患者的血清肌酐水平大于或等于1.5 mg / dL男性或1.4 mg / dL的女性。在满足这些患者血清肌酐水平,不启动或继续INVOKAMET如果eGFR持续小于45 mL / min / 1.73平方米(见禁忌症(4)和警告和注意事项(5.3)]。不需要剂量调整INVOKAMET轻度肾功能障碍患者(60毫升/分钟/ 1.73平方米的表皮生长因子受体或更大)。限制INVOKAMET canagliflozin 50毫克的剂量每天两次中度肾功能损害患者的eGFR 45到不到60毫升/分钟/ 1.73平方米。2.3同时使用UDP-Glucuronosyl转移酶(UGT)酶诱导物
如果ugt的诱导物(如利福平、苯妥英、镇静安眠剂,例如)与INVOKAMET流行性流感减毒活疫苗,考虑增加canagliflozin 150毫克的剂量每天两次在患者目前容忍50毫克,每日两次60 mL / min / 1.73平方米的表皮生长因子受体或更高,需要额外的血糖控制(见药物相互作用(7.2))。
考虑另一个患者的降糖药eGFR 45到不到60毫升/分钟/ 1.73平方米UGT诱导物,接受并发治疗。
-

Meloxicam
![Meloxicam Tablet [Pd-rx Pharmaceuticals, Inc.] Meloxicam平板(Pd-rx制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=2524b253-069e-4028-819c-361b888df110&name=ortho-04.jpg)
达到最大的避孕效果,ORTHO-NOVUM®平板电脑和莫迪康®平板电脑必须完全按照指示和间隔不超过24小时。ORTHO-NOVUM®平板电脑和莫迪康®平板电脑可用的DIALPAK®平板电脑自动售货机预置一个星期天开始。第一天开始也可以。
周日开始
当把ORTHO-NOVUM®7/7/7, ORTHO-NOVUM®1/35,和莫迪康®,首先应采取“积极”平板电脑在月经开始后的第一个星期日。如果周日开始,第一个应该采取“积极”的平板电脑。每天一个活动平板21天之后,一个绿色的“提醒”平板电脑每天7天。已经采取了28个平板电脑后,新课程开始第二天(周日)。第一周期的周日开始养生法,另一种方法避孕应该使用避孕套或杀精剂等直到第一个连续7天的管理。
如果病人错过一个(1)“活跃”平板电脑在周1、2或3,平板电脑应该只要她记得。如果病人错过两(2)“活跃”平板电脑在1或2周,病人应该采取两(2)平板电脑一天她记得和两(2)平板电脑第二天;然后继续每天服用一(1)平板电脑,直到她完成。这个病人应该指示使用备份的方法避孕,如避孕套或杀精剂如果她有性爱后的七(7)天失踪的药丸。如果病人错过两(2)“活跃”平板电脑在第三周或错过三(3)以上连续“活跃”平板电脑,病人应该继续每天服用一片,直到星期天。周日的病人应该扔掉其余的包,并开始一个新的包。这个病人应该指示使用备份的方法避孕,如果她有性爱后的七(7)天失踪的药丸。
完成指令来促进患者咨询适当的药物使用可能详细的病人中发现标签(“如何服用避孕药”部分)。
第一天开始
的用量ORTHO-NOVUM®7/7/7, ORTHO-NOVUM®1/35,和莫迪康®,初始周期疗法,是一种“积极”平板电脑管理每日从1日到21天的月经周期,计算月经的第一天作为“第一天”紧随其后的是一个绿色的“提醒”平板电脑每天7天。平板电脑不间断地为28天。28平板电脑后,第二天开始一个新的课程。
如果病人错过一个(1)“活跃”平板电脑在周1、2或3,平板电脑应该只要她记得。如果病人错过两(2)“活跃”平板电脑在1或2周,病人应该采取两(2)平板电脑一天她记得和两(2)平板电脑第二天;然后继续每天服用一(1)平板电脑,直到她完成。这个病人应该指示使用备份的方法避孕,如避孕套或杀精剂如果她有性爱后的七(7)天失踪的药丸。如果病人错过两(2)“活跃”平板电脑在第三周或错过三(3)以上连续“活跃”平板电脑,病人应该扔掉其余的包,并开始一个新的包。这个病人应该指示使用备份的方法避孕,如果她有性爱后的七(7)天失踪的药丸。
完成指令来促进患者咨询适当的药物使用可能详细的病人中发现标签(“如何服用避孕药”部分)。
使用ORTHO-NOVUM®7/7/7, ORTHO-NOVUM®1/35,和莫迪康®对于避孕可能发起4周产后女性选择不进行母乳喂养。当平板电脑管理在产后时期,血栓栓塞疾病的风险增加相关的产后必须考虑。(见禁忌症和警告有关血栓栓塞疾病。参见预防措施:哺乳期妇女。)排卵的可能性和概念开始之前应考虑药物治疗。
(见讨论口服避孕药的剂量相关性血管疾病的风险。)
-

Doribax
![Doribax (Doripenem) Powder, For Solution [Janssen Pharmaceuticals, Inc.] Doribax (Doripenem)粉,为解决方案(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=ded65c55-db1c-4dab-a707-951e7cc87c79&name=doribax-03.jpg)
2.1推荐剂量
的推荐剂量DORIBAX®500毫克每8小时管理由静脉注入了一个多小时的病人≥18岁。推荐剂量和管理由感染是表1所示:
表1:剂量的DORIBAX®由感染感染剂量频率灌注时间(小时)时间*时间包括可能切换到一个适当的口服治疗,经过至少3天的肠外治疗,一旦临床改善。†持续时间可以延长到14天患者并发菌血症。复杂腹腔感染500毫克每8小时1为5 - 14天*复杂的泌尿道感染,包括肾盂肾炎500毫克每8小时1 * 10天2.2患者肾功能损害
表2:剂量的DORIBAX®患者的肾功能损害估计CrCl(毫升/分钟)推荐的给药方案DORIBAX®*(参见准备250毫克DORIBAX®使用250毫克剂量250毫克的瓶和制备DORIBAX®使用500毫克剂量瓶(2.3)> 50没有必要剂量调整≥30≤50 250毫克*每8小时进行静脉注射(超过1小时)> 10 < 30 250毫克*管理静脉注射(超过1小时)每12小时下面的公式可以用来估计CrCl。公式中使用血清肌酐应该表示肾功能的稳定状态。
男性:肌酐清除率(毫升/分钟)=重量(公斤)×在岁(140 -)72×血清肌酐(mg / dL)雌性:肌酐清除率(mL / min) = 0.85×值计算DORIBAX®hemodialyzable;然而,没有足够的信息在血透患者中剂量调整的建议。
2.3准备的解决方案
DORIBAX®不含抑菌防腐。无菌技术必须遵循在输液的准备。
准备DORIBAX注入在巴克斯特Minibag加上™输液袋咨询输液袋制造商的指示。
注射用药物的药物产品应检查视觉颗粒物和变色之前使用时解决方案和容器许可证。DORIBAX注资范围不清楚,无色的解决方案,解决方案清晰和略黄。这个范围内的颜色的变化不影响产品的效力。
准备500毫克DORIBAX®剂量使用500毫克瓶
构成了500毫克瓶10毫升无菌注射用水或0.9%氯化钠注射液(生理盐水),轻轻摇悬挂。合成的浓度大约是50毫克/毫升。警告:构成悬挂不是直接注入。撤回暂停用一个注射器针和21个指标将其添加到一个输液袋包含100毫升生理盐水或5%葡萄糖;轻轻摇晃,直到清晰。最后输液浓度大约是4.5毫克/毫升。准备250毫克DORIBAX®剂量使用250毫克瓶
构成了250毫克瓶10毫升无菌注射用水或0.9%氯化钠注射液(生理盐水),轻轻摇悬挂。合成的浓度大约是25毫克/毫升。警告:构成悬挂不是直接注入。撤回暂停用一个注射器针和21个指标将其添加到一个包含50或100毫升的输液袋的生理盐水或5%葡萄糖;轻轻摇晃,直到清晰。最后输液浓度大约是4.2毫克/毫升(50 mL输液袋)或大约2.3毫克/毫升(100毫升输液袋)。准备250毫克DORIBAX®剂量使用500毫克瓶
构成了500毫克瓶10毫升无菌注射用水或0.9%氯化钠注射液(生理盐水),轻轻摇悬挂。合成的浓度大约是50毫克/毫升。警告:构成悬挂不是直接注入。撤回暂停用一个注射器针和21个指标将其添加到一个输液袋包含100毫升生理盐水或5%葡萄糖;轻轻摇晃,直到清晰。删除55毫升的袋子,丢弃这个解决方案。注入剩余的解决方案,其中包含250毫克(大约4.5毫克/毫升)。2.4兼容性
的兼容性DORIBAX®和其他药物尚未建立。DORIBAX®不应该混合包含其他药物或身体添加到解决方案。
2.5存储构成解决方案的
在宪法和无菌注射用水或0.9%氯化钠(生理盐水)注射,DORIBAX悬瓶可能举行的小时之前转移和稀释的输液袋。
稀释后的悬架与生理盐水或5%葡萄糖,DORIBAX注入储存在室温下或在制冷应该根据表3次完成。
表3:存储和稳定的注入方案准备在正常生理盐水或5%葡萄糖注入稳定时间在房间里临时准备。(包括室温储存和注入时间)稳定在2 - 8°C(制冷)(包括冰箱存储和注入时间)5%葡萄糖生理盐水12小时72小时4小时24小时构成DORIBAX暂停或DORIBAX注入不应该冻结。这个存储信息也适用于DORIBAX®稀释在巴克斯特Minibag加上™。
-

Firmagon
![Firmagon (Degarelix) Kit [Ferring Pharmaceuticals Inc.] Firmagon (Degarelix)工具包(显示出制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=384e7a40-dcbd-4908-bf5e-65abc9932973&name=ortho-27.jpg)
2.1如何开始ORTHO-CYCLEN或邻位的TRI-CYCLEN
ORTHO-CYCLEN和邻位TRI-CYCLEN分发DIALPAK平板电脑自动售货机或VERIDATE平板电脑自动售货机(参见如何提供/存储和处理(16)]。ORTHO-CYCLEN和邻位的TRI-CYCLEN可能开始使用第一天开始或周日开始(见表1)。第一个周期的周日开始养生法,应该使用一个额外的避孕方法,直到第一个连续7天的管理。
2.2如何ORTHO-CYCLEN或邻位的TRI-CYCLEN
表1:说明政府ORTHO-CYCLEN或邻位的TRI-CYCLEN完成指令来促进患者咨询适当的平板电脑上使用位于fda批准的病人标识。女性开始COCs目前未使用激素避孕(第一天开始或星期天开始)
重要:考虑排卵的可能性和概念开始之前这种产品。
平板电脑颜色:ORTHO-CYCLEN活跃的平板电脑是蓝色的(每天1 - 21)。昊图公司TRI-CYCLEN活跃的平板电脑是白色的(每天1 - 7),浅蓝色(每天8 - 15)和蓝色(每天16 - 21)。ORTHO-CYCLEN和邻位的TRI-CYCLEN都有深绿色的平板电脑(每天22到28)。第一天开始:第一次活动平板不考虑膳食在月经的第一天。同时采取后续活动平板电脑一旦每日每天总共21天。每天取一个深绿色不活跃的平板电脑7天,同时,活跃的平板电脑。开始一周的每个后续包在同一天第一周期包(即。当天,在最后一个不活跃的平板电脑)周日开始:采取第一个主动平板不考虑吃饭在月经开始后的第一个星期日。由于怀孕的潜在风险,使用额外的无激素避孕方法(如避孕套和杀精剂)的前七天病人的第一个周期群ORTHO-CYCLEN或邻位的TRI-CYCLEN。同时采取后续活动平板电脑一旦每日每天总共21天。 Take one dark green inactive tablet daily for the following 7 days and at the same time of day that active tablets were taken. Begin each subsequent pack on the same day of the week as the first cycle pack (i.e., on the Sunday after taking the last inactive tablet) and additional non-hormonal contraceptive is not needed. Switching to ORTHO-CYCLEN or ORTHO TRI-CYCLEN from another oral contraceptive Start on the same day that a new pack of the previous oral contraceptive would have started. Switching from another contraceptive method to ORTHO-CYCLEN or ORTHO TRI-CYCLEN Start ORTHO-CYCLEN or ORTHO TRI-CYCLEN: Transdermal patch On the day when next application would have been scheduled Vaginal ring On the day when next insertion would have been scheduled Injection On the day when next injection would have been scheduled Intrauterine contraceptive On the day of removal If the IUD is not removed on first day of the patient's menstrual cycle, additional non-hormonal contraceptive (such as condoms and spermicide) is needed for the first seven days of the first cycle pack. Implant On the day of removal开始ORTHO-CYCLEN或邻位的TRI-CYCLEN堕胎后或流产
对于妊娠前三个月
孕早期流产后或流产,ORTHO-CYCLEN或邻位的TRI-CYCLEN可能立即开始。不需要额外的避孕方法如果ORTHO-CYCLEN或邻位的TRI-CYCLEN立即启动。如果ORTHO-CYCLEN或邻位的TRI-CYCLEN不是开始后5天内终止妊娠,病人应该使用额外的无激素避孕方法(如避孕套和杀精剂)的前七天她第一次循环群ORTHO-CYCLEN或邻位的TRI-CYCLEN。中期妊娠
才开始后4周中期妊娠流产或流产,由于血栓栓塞疾病的风险增加。之后,开始ORTHO-CYCLEN或邻位的TRI-CYCLEN指令表1中第一天或者周日开始,。如果使用周日开始,使用额外的无激素避孕方法(如避孕套和杀精剂)的前七天病人的第一个周期群ORTHO-CYCLEN或邻位的TRI-CYCLEN。(见禁忌症(4)、警告和注意事项(5.1),和fda批准的病人标签。)在分娩后开始ORTHO-CYCLEN或邻位的TRI-CYCLEN
才开始后4周交货,由于血栓栓塞疾病的风险增加。后开始避孕治疗与ORTHO-CYCLEN或邻位的TRI-CYCLEN指令表1中对女性没有使用激素避孕。ORTHO-CYCLEN或邻位的TRI-CYCLEN不推荐哺乳期妇女使用(见使用在特定的人群(8.3))。如果女人没有一个产后时期,考虑排卵的可能性和概念使用ORTHO-CYCLEN或邻位TRI-CYCLEN之前发生。(见禁忌症(4)、警告和注意事项(5.1),使用特定的人群(8.1和8.3),和fda批准的病人标识)。DIALPAK®平板电脑自动售货机:
设置一天:□第一天开始:打开拨空DIALPAK直到箭头指向的第一天,病人的时期。□周日开始:空DIALPAK上的箭头应指向苏(周日)。插入新添排队添上的“V”形和“V”形的顶部DIALPAK。快速补充。丸“1”准备。总是开始与丸丸循环“1”所示内填满环的一部分。删除药丸通过压低服用避孕药的“1”。避孕药会通过一个洞DIALPAK的后面。病人应该等待24小时下药丸。把药丸”2、“打开拨号DIALPAK第二天在顺时针方向。 Continue to take one pill each day until all the pills have been taken. Turn the dial to the pill "1" position to remove the empty refill and insert a new refill. The first pill in every refill will always be taken on the same day of the week, no matter when the patient's next period starts.VERIDATE®平板电脑自动售货机
地方的补充VERIDATE平板电脑分发器,以便补充V缺口是顶部的分配器。按补充下适合坚定下所有的大人物(见下面的例子)。周日如果病人开始服药,应采取第一个活跃的药丸的患者的月经期后的第一个星期日开始。删除第一个活跃的药丸顶部的分配器(周日)按避孕药通过分发器的底部的洞。ORTHO-CYCLEN:
如果病人将开始吃药“第一天”,选择对应的蓝色药片一天的星期病人将第一个药丸。删除,蓝色药片按避孕药通过分发器的底部的洞。昊图公司TRI-CYCLEN:
如果病人将开始服药一天除了周日,日历标签提供了,应该放在日历VERIDATE的中心。将正确的标签,确定正确的开始一天,找到那一天印在蓝色的标签上,并当天第一个白色药片直属V缺口顶部的分配器。删除标签的支持。新闻中心的标签在印刷日历的中心。去除白色药片按避孕药通过分发器的底部的洞。已经采取了所有的深绿色药片后,插入一个新的补充到VERIDATE。病人应采取第一药第二天,即使病人的周期还没有结束。插入新添(ORTHO-CYCLEN或邻位的TRI-CYCLEN):
电梯的空填满VERIDATE平板分发器。插入新的补充,补充的V形切口顶部的分配器。按补充下适合坚定地大人物。2.3没有平板电脑
表2:说明了ORTHO-CYCLEN或邻位的TRI-CYCLEN平板电脑如果一活跃的平板电脑是错过了周1,2,或者3平板电脑尽快。继续每天服用一片,直到包完成。如果两个活跃的平板电脑是错过了周1或2花两个星期错过了平板电脑尽快第二天和接下来的两个活跃的平板电脑。继续每天服用一片,直到包完成。额外的无激素避孕方法(如避孕套和杀精剂)应该作为备用后7天内如果病人性缺失的平板电脑。如果两个活动平板电脑是错过了在第三周或三个或更多活跃的平板电脑连续错过了周1,2或3天1开始:扔掉其余的包,并开始一个新的包。周日开始:继续每天服用一片,直到周日,然后扔掉其余的包,并开始一个新的包。额外的无激素避孕方法(如避孕套和杀精剂)应该作为备用后7天内如果病人性缺失的平板电脑。2.4建议肠胃紊乱
在严重的呕吐或腹泻的情况下,吸收可能不完整的和额外的应采取避孕措施。如果发生呕吐或腹泻后3 - 4小时内采取积极的平板电脑,处理这个问题作为一个错过了平板电脑(参见fda批准的病人标识)。
2.5 ORTHO-TRICYCLEN用于痤疮
时间的起始剂量的邻位的TRI-CYCLEN痤疮应该遵循使用指南的邻位的TRI-CYCLEN作为口服避孕药。beplay体验参考剂量和管理部分(2.1)的指令。
-

昊图公司除了
![Ortho Cept (Desogestrel And Ethinyl Estradiol) Kit [Janssen Pharmaceuticals, Inc.] 昊图公司除了(去氧孕烯炔雌醇)工具包(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=a7140182-a0ac-485e-929c-6e05092c2ae5&name=ortho-04.jpg)
达到最大的避孕效果,ORTHO-CEPT®必须完全按照指示和间隔不超过24小时。ORTHO-CEPT®可用在吸塑卡平板电脑自动售货机预置一个星期天开始。第一天开始。
第一天开始
的用量ORTHO-CEPT®的初始周期疗法是一个光橙色“活跃”平板电脑管理每日从第一天到21天的月经周期,计算月经的第一天作为“第一天”。平板电脑没有打扰的采取如下:一个光橙色“活跃”平板电脑每天21天,然后一个绿色的“提醒”平板电脑每天7天。已经采取了28个平板电脑后,新课程开始和浅橙色的“活跃”平板电脑是第二天了。
使用ORTHO-CEPT®对于避孕可能发起4周产后女性选择不进行母乳喂养。当平板电脑管理在产后时期,血栓栓塞疾病的风险增加相关的产后必须考虑。(见禁忌症和警告有关血栓栓塞疾病。参见预防措施:哺乳期妇女。)如果病人开始ORTHO-CEPT®产后,尚未有一个时期,她应该要求使用另一种方法避孕,直到光橙色“活跃”平板电脑已经被每天7天。排卵的可能性和概念开始之前应考虑药物治疗。如果病人错过一个(1)光橙色“积极”平板电脑在周1,2或3,光橙色应采取“积极”平板电脑一旦她回忆道。如果病人错过两(2)光橙色“活跃”平板电脑在1或2周,病人应该采取两(2)光橙色“活跃”平板电脑一天她记得和两(2)光橙色“活跃”平板电脑第二天;然后继续采取一(1)光橙色“活跃”平板电脑一天,直到她完成。这个病人应该指示使用备份的方法避孕,如避孕套或杀精剂如果她有性爱后的七(7)天失踪的药丸。 If the patient misses two (2) light orange "active" tablets in the third week or misses three (3) or more light orange "active" tablets in a row, the patient should throw out the rest of the pack and start a new pack that same day. The patient should be instructed to use a back-up method of birth control if she has sex in the seven (7) days after missing pills.
周日开始
时ORTHO-CEPT®,第一个光橙色应采取“积极”平板电脑在月经开始后的第一个星期日。如果周日开始,第一个光橙色“活跃”平板电脑是在那一天。如果直接从另一个口服避孕药,切换第一光橙色应采取“积极”平板电脑后第一个星期日之前的最后活跃的平板电脑产品。平板电脑没有打扰的采取如下:一个光橙色“活跃”平板电脑每天21天,然后一个绿色的“提醒”平板电脑每天7天。已经采取了28个平板电脑后,新课程开始和浅橙色的“活跃”平板电脑是第二天(周日)。当启动周日开始方案时,应该使用另一种方法避孕,直到第一个连续7天的管理。
使用ORTHO-CEPT®产后避孕可能发起4周。当平板电脑管理在产后时期,血栓栓塞疾病的风险增加相关的产后必须考虑。(见禁忌症和警告有关血栓栓塞疾病。参见预防措施:哺乳期妇女。)如果病人开始ORTHO-CEPT®产后,尚未有一个时期,她应该要求使用另一种方法避孕,直到光橙色“活跃”平板电脑已经被每天7天。排卵的可能性和概念开始之前应考虑药物治疗。如果病人错过一个(1)光橙色活跃平板在周1,2或3,光橙色应采取“积极”平板电脑一旦她回忆道。如果病人错过两(2)光橙色“活跃”平板电脑在1或2周,病人应该采取两(2)光橙色“活跃”平板电脑一天她记得和两(2)光橙色“活跃”平板电脑第二天;然后继续采取一(1)光橙色“活跃”平板电脑一天,直到她完成。这个病人应该指示使用备份的方法避孕,如避孕套或杀精剂如果她有性爱后的七(7)天失踪的药丸。 If the patient misses two (2) light orange "active" tablets in the third week or misses three (3) or more light orange "active" tablets in a row, the patient should continue taking one light orange "active" tablet every day until Sunday. On Sunday the patient should throw out the rest of the pack and start a new pack that same day. The patient should be instructed to use a back-up method of birth control if she has sex in the seven (7) days after missing pills.
所有剂量方案附加指令
出血,和频繁的原因是闭经患者,由于口服避孕药。突破性出血,在所有情况下的不规则阴道出血,功能性原因应该牢记。在未确诊的持续或复发性异常阴道出血,足够的诊断措施表示排除妊娠或恶性肿瘤。如果病理被排除在外,或者改变到另一个配方可能解决这个问题。改变一个口服避孕药雌激素含量更高,虽然可能有助于减少月经不规则,应该只在必要时因为这可能会增加血栓栓塞疾病的风险。
使用口服避孕药在发生错过月经期:
如果病人没有遵守规定的时间表,应该考虑怀孕的可能性的时候第一次错过了时间和口服避孕药使用应该停止如果怀孕被证实。如果病人坚持规定的方案,错过两个连续的时期,应该排除怀孕。 -

Pancreaze
![Pancreaze (Pancrelipase) Capsule, Delayed Release [Janssen Pharmaceuticals, Inc.] Pancreaze(胰脂肪酶)胶囊,推迟发布(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=e1431edd-0fc5-4ebc-8c10-53deb0db0d23&name=pancreaze-01.jpg)
2.1剂量
PANCREAZE不是可互换与其他胰脂肪酶产品。
PANCREAZE口头管理。治疗应该最低的推荐剂量开始,逐渐增加。PANCREAZE的用量应该是个性化的基于临床症状,脂肪痢的程度,和脂肪含量的饮食(参见下面的剂量限制)。
用量对胰酶替代治疗的建议发表后囊性纤维化基金会Conferences.1共识,2、3 PANCREAZE应该管理的方式一致的建议,会议中提供以下段落。患者可能给身体脂肪ingestion-based或实际体重依赖型剂量给药方案。
婴儿(12个月)
婴儿会给2000到4000脂肪酶单位每120毫升的配方奶或母乳喂养。不要混合PANCREAZE胶囊内容直接进入配方奶或母乳之前政府(见剂量和管理(2.2))。
孩子年龄超过12个月,不到4年
酶剂量应该从1000年开始脂肪酶单位/千克的体重每顿饭不到4岁儿童最多2500脂肪酶单位/公斤体重/餐(或小于或等于10000脂肪酶单位/公斤体重/天),或少于每天4000脂肪酶单位/克脂肪摄入。
4岁及以上儿童和成人
酶剂量应该从500年开始脂肪酶单位/千克的体重每顿饭对于那些年龄超过4岁最多2500脂肪酶单位/公斤体重/餐(或小于或等于10000脂肪酶单位/公斤体重/天),或少于每天4000脂肪酶单位/克脂肪摄入。
通常,一半的处方剂量PANCREAZE整整一个个性化的膳食应该给每个小吃。每日总剂量应该反映大约每天三餐+两个或三个小吃。
表示为脂肪酶酶剂量单位/千克的体重每顿饭应该减少老年患者因为他们更重,但倾向于摄入更少的脂肪每公斤体重。
限制剂量
剂量不应超过推荐的最大剂量设定的囊性纤维化基金会共识会议Guidelines.1, 2、3beplay体验
如果脂肪痢持续的症状与体征,剂量可能增加了医疗保健专业。患者应该被指示不要增加剂量。有伟大的inter-individual反应酶的变化;因此,建议的剂量范围。用量的变化可能需要几天的调整时期。如果剂量超过2500脂肪酶单位/千克的体重每顿饭,进一步调查是十分必要的。
剂量超过2500脂肪酶单位/千克的体重每顿饭(或大于10000脂肪酶单位/公斤体重/天)应小心使用,只有在有效的记录三天粪便脂肪的措施表明显著提高脂肪的吸收系数。剂量大于6000脂肪酶单位/千克的体重每顿饭已经与结肠狭窄有关,表明fibrosing colonopathy,儿童与囊性纤维化少于12岁(见警告和注意事项(5.1))。目前患者接受高剂量超过6000脂肪酶单位/千克的体重每顿饭应该检查和剂量立即减少或滴定下降到一个较低的范围内。
2.2政府
PANCREAZE规定应该被视为一个医疗保健专业。
婴儿(12个月)
PANCREAZE应立即婴儿每次喂食前,使用剂量的2000到4000脂肪酶单位每120毫升的配方奶或母乳喂养。胶囊的内容可能是撒在少量的软食物酸性pH值为4.5或更低(例如,苹果酱)和婴儿在15分钟内。胶囊也可以直接管理的内容。政府应遵循由母乳或配方。胶囊的内容不应直接混合配方奶或母乳,因为这可能会降低疗效。应该小心以确保PANCREAZE不是碎或者嚼在口中留存,以避免刺激口腔黏膜。
儿童和成人
PANCREAZE应采取在食物或零食,有足够的液体。PANCREAZE胶囊,胶囊内容不应该被碾碎或咀嚼。胶囊应该整个吞下。
的患者无法接受完整的胶囊,胶囊可能会小心翼翼地打开,里面的东西撒在少量的软食物酸性pH值为4.5或更低(例如,苹果酱)。PANCREAZE-soft食品混合物应立即吞下没有破碎或咀嚼,与水或果汁,确保完整的摄入。应该小心,以确保不保留在口腔药物。
-

Haldol癸酸盐
![Haldol Decanoate (Haloperidol Decanoate) Injection [Janssen Pharmaceuticals, Inc.] Haldol癸酸盐(氟哌啶醇癸酸酯)注入(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=af0159a8-dff5-449a-aa2b-a0c430081e21&name=haldol-06.jpg)
HALDOL癸酸盐50和HALDOL癸酸盐100应该由深肌内注射。建议21计针。每个注射部位的最大容积不应超过3毫升。不管理静脉注射。
注射用药物的药物产品应检查视觉颗粒物和变色政府之前,每当解决方案和容器许可证。
HALDOL癸酸盐50和100年HALDOL癸酸酯用于精神分裂症患者需要长期肠外抗精神病治疗。这些病人应该在抗精神病药物之前稳定之前考虑转换为氟哌啶醇癸酸盐。此外,建议患者被认为是氟哌啶醇癸酸盐疗法治疗,和容忍,短效HALDOL(氟哌啶醇)为了减少意外不良对氟哌啶醇的可能性。密切临床监督需要初始剂量调整期间为了减少过剂量的风险或再现下注射前的精神病症状。在调整剂量或事件恶化的症状的精神分裂症,氟哌啶醇癸酸盐治疗可以用短效补充形式的氟哌啶醇。
的剂量HALDOL癸酸盐50或HALDOL应该表达的氟哌啶醇癸酸盐100的内容。起始剂量的氟哌啶醇癸酸盐应根据病人的年龄、病史、身体状况,应对前抗精神病治疗。确定最低有效剂量的首选的方法是开始较低的初始剂量并根据需要向上调整剂量。对病人之前保持在低剂量的抗精神病药物(如相当于10毫克/天口服氟哌啶醇),建议初始剂量的氟哌啶醇癸酸盐前10 - 15倍剂量口服氟哌啶醇等价物;有限的临床经验表明,较低的初始剂量可能是足够的。
最初的治疗
转换从口服氟哌啶醇、氟哌啶醇癸酸盐可以通过使用一个初始剂量的氟哌啶醇癸酸盐10到20倍之前的每日剂量口服氟哌啶醇等价物。
在疲惫不堪的老年患者,或稳定的低剂量的口服氟哌啶醇(例如相当于10毫克/天口服氟哌啶醇),一系列的10到15倍之前的每日剂量口服氟哌啶醇等价物适合初始转换。
在病人之前保持更高的剂量抗精神病药物来说,低剂量的方法复发风险的精神病患者的呼吸困难和长期使用氟哌啶醇导致药物的耐受性,前面的20倍剂量口服氟哌啶醇等价物首次转换,应考虑与下行滴定成功注射。
初始剂量的氟哌啶醇癸酸盐不应超过100毫克,不管以前抗精神病剂的要求。因此,如果转换需要超过100毫克氟哌啶醇癸酸盐作为初始剂量,剂量应在两个注射,即最多100毫克最初紧随其后的平衡在3 - 7天。
维持治疗
维持剂量的氟哌啶醇癸酸盐必须与滴定向上或向下基于个性化的治疗反应。通常的维护范围是10到15次之前的每日剂量口服氟哌啶醇等价物依赖病人的临床反应。
HALDOL癸酸盐剂量建议病人Monthly1st月维护稳定低每日口服剂量(10毫克/天)老年或疲惫不堪的10 - 15前10 - 15××每日口服剂量每日口服剂量高复发doseRisk 20×每日口服剂量10 - 15×先前每日口服剂量口服氟哌啶醇的宽容密切临床监督需要在启动和稳定的氟哌啶醇癸酸酯治疗。氟哌啶醇癸酸盐通常是管理每月或每4周。然而,病人反应的变化可能决定需要调整剂量间隔以及剂量(见临床药理学)。
临床经验与氟哌啶醇癸酸酯在每月超过450毫克剂量是有限的。
说明打开安瓿
1。药物治疗往往掌握在安瓿的顶部。打破了之前安瓿,轻轻用手指轻击安瓿的顶部,直到所有液体底部的安瓿移。安瓿有彩色环(s)和彩色点艾滋病打破安瓿时手指的位置。步骤12。把拇指和食指之间的安瓿的彩色点面对你。步骤23所示。另一只手的食指位置支持安瓿的脖子。拇指位置以便它涵盖了彩色点和平行于彩色环(年代)。步骤34所示。保持彩色点上的拇指和食指近,申请公司彩色点压力的方向箭头折断安瓿开放。步骤4 -

Asacol
![Asacol (Mesalamine) Tablet, Delayed Release [Warner Chilcott (Us), Llc] Asacol (Mesalamine)平板电脑,推迟发布(华纳齐克特(美国)有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=27cfe684-7d11-4f37-9c8b-b2bdd6b5348e&name=haldol-06.jpg)
有相当大的变化从病人的病人所需的药物治疗。正如所有药物用于治疗精神分裂症,剂量应个体化根据每个病人的需求和响应。剂量调整,向上或向下,应尽可能快速可行的实现最佳治疗控制。
确定初始剂量,应该考虑病人的年龄、疾病的严重程度,以前的响应其他抗精神病药物,和任何伴随的药物或疾病状态。疲惫不堪的或老年病人,以及那些历史的抗精神病药物的不良反应,可能需要更少的HALDOL(氟哌啶醇)。最优反应这样的患者通常是获得更加渐进的剂量调整和较低的剂量水平。
肠外治疗,肌肉在5毫克剂量的2,用于提示控制十分激动的精神分裂症患者中度严重的症状非常严重。根据病人的反应,随后的剂量可以,管理通常每小时,虽然每隔4到8小时可能是令人满意的。最大剂量为20毫克/天。
对照试验建立肌肉的政府在儿童的安全性和有效性尚未进行。
注射用药物的药物产品应检查视觉颗粒物和变色政府之前,每当解决方案和容器许可证。
切换过程
口头形式应该取代注射尽快。在缺乏生物利用度研究之间建立生物等效性这两个剂型为剂量提出以下指导方针。beplay体验初始近似的每日总剂量要求,注射剂量前24小时可用。因为这个剂量只是初步估计,建议仔细监测的临床症状和体征,包括临床疗效、镇静,和不良反应,定期进行第一几天后开始切换。通过这种方式,剂量调整,向上或向下,可以快速完成。根据病人的临床状态,第一个口服剂量应给予后12 - 24小时内注射用药物的剂量。
说明打开安瓿
1。药物治疗往往掌握在安瓿的顶部。打破了之前安瓿,轻轻用手指轻击安瓿的顶部,直到所有液体底部的安瓿移。安瓿有彩色环(s)和彩色点艾滋病打破安瓿时手指的位置。步骤12。把拇指和食指之间的安瓿的彩色点面对你。步骤23所示。另一只手的食指位置支持安瓿的脖子。拇指位置以便它涵盖了彩色点和平行于彩色环(年代)。步骤34所示。保持彩色点上的拇指和食指近,申请公司彩色点压力的方向箭头折断安瓿开放。步骤4 -

Nucynta
![Nucynta (Tapentadol Hydrochloride) Tablet, Film Coated [Janssen Pharmaceuticals, Inc.] Nucynta(盐酸Tapentadol)平板电脑,薄膜涂层(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=00a8921e-46a6-4df1-a744-9e532b6fb06f&name=nucynta-04.jpg)
2.1个性化的剂量
与任何阿片类药物产品,单独为每个病人调整给药方案,考虑到病人的镇痛治疗经验。在tapentadol初始剂量的选择,注意以下几点:
每日总剂量,阿片类药物的效力和具体特征患者已经服用之前;相对效力的可靠性估计所需的用来计算等效硫酸吗啡剂量;阿片类药物耐受的病人的程度;病人的一般情况和医疗状况;并发的药物;病人的疼痛的类型和严重性;风险因素滥用成瘾或转移,包括之前的滥用的历史中,成瘾或转移。以下推荐剂量,因此,只能被视为建议方法实际上是一个随着时间的推移的一系列临床决策的管理每个病人的痛苦。
不断重新评估病人的接受tapentadol很重要,特别注意维护疼痛控制和副作用的相对发病率与治疗有关。
在长期治疗,特别是对于non-cancer-related疼痛,定期评估持续使用阿片类止痛药的必要性。
期间改变镇痛需求,包括最初的滴定,频繁接触之间的推荐医生,医疗团队的其他成员,病人和照顾者/家庭。监测病人呼吸道或中枢神经系统抑郁的迹象。
2.2开始治疗
剂量50毫克,75毫克,或100毫克每4至6小时根据疼痛强度。
第一天的剂量,第二剂量可能管理第一剂量后一个小时,如果没有达到足够的疼痛与第一剂量。后续计量是50毫克,75毫克,或100毫克每4至6小时,应该进行调整,以保持足够的镇痛与可接受的耐受性。
每日剂量大于700毫克第一天的治疗和600毫克在随后的日子还没有被研究过,不推荐。
NUCYNTA®可以有或没有食物(见临床药理学(12.3))。
2.3肾功能损害
使用NUCYNTA®有严重肾功能损害的患者不建议(见警告和注意事项(5.16)和临床药理学(12.3)]。
不推荐剂量调整患者的轻度或中度肾功能损害。
2.4肝损伤
的安全性和有效性NUCYNTA®还没有研究对严重肝损伤患者(儿童得分10 - 15)和使用在这个人口不推荐(见警告和注意事项(5.15))。
启动治疗对中度肝损伤患者与50毫克(儿童得分7 - 9)没有比每8小时更频繁(最多三个剂量在24小时内)。进一步治疗应该反映维护可接受的耐受性的镇痛是通过缩短或者延长给药间隔(见临床药理学(12.3))。
不推荐剂量调整患者的轻度肝损害(儿童得分5到6)(见临床药理学(12.3))。
2.5老年病人
一般来说,推荐剂量老年病人与正常肾和肝脏功能是一样的年轻成人患者与正常肾和肝脏功能。因为老年患者更有可能减少肾和肝脏功能,应该考虑从老年患者较低的推荐剂量范围。
2.6停止治疗
当病人与tapentadol不再需要治疗,逐渐减少剂量,防止戒断症状和体征病人身体上的依赖(见警告和注意事项(5.13))。
-

Nucynta呃
![Nucynta Er (Tapentadol Hydrochloride) Tablet, Film Coated, Extended Release [Janssen Pharmaceuticals, Inc.] Nucynta Er(盐酸Tapentadol)平板电脑,涂膜,延长释放(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=f4c911f3-484b-44fa-833e-2d970d39be8f&name=nucynta-05.jpg)
2.1初始计量
NUCYNTA®ER规定只有通过医疗保健专业人士应该知识渊博的强效阿片类药物的使用对慢性疼痛的管理。
单独启动每个患者的给药方案,考虑到病人的镇痛治疗经验和成瘾的风险因素,滥用和误用(见警告和注意事项(5.1))。密切监测患者呼吸道抑郁症,特别是24 - 72小时内开始治疗NUCYNTA®ER(见警告和注意事项(5.2))。
必须采取NUCYNTA®ER平板电脑。破碎、咀嚼或溶解NUCYNTA®ER平板电脑将导致控制交付tapentadol和可能导致过量或死亡(见警告和注意事项(5.2))。
NUCYNTA®ER管理每日两次的频率(每12个小时)。
停止所有其他tapentadol和曲马多产品时开始和NUCYNTA®ER(见警告和注意事项(5.10))。虽然最大批准每日总剂量NUCYNTA®速是每天600毫克,最大每日总剂量的NUCYNTA®ER是500毫克。不超过每日总剂量的NUCYNTA®500毫克的ER。
使用NUCYNTA®ER第一阿片类止痛剂
启动治疗NUCYNTA®ER 50毫克平板电脑每天两次口头(大约每12小时)。
使用NUCYNTA®急诊室的病人不是阿片类宽容
的起始剂量的患者不阿片类宽容NUCYNTA®ER 50毫克口服每天两次(大约每12小时)。开始使用高剂量的病人不是阿片类宽容可能会引起致命的呼吸道抑郁。阿片类药物的病人宽容那些接受,一个星期或更久,每天至少60毫克口服吗啡,25微克每小时皮肤芬太尼,每天30毫克口服羟考酮,8毫克口服hydromorphone每天25毫克每天口服羟吗啡酮或equianalgesic另一个阿片类药物的剂量。
转换从NUCYNTA®, NUCYNTA®
病人可以从NUCYNTA转换®,NUCYNTA®ER使用每日总剂量相当于NUCYNTA®分裂成两个相等的剂量的NUCYNTA®ER相隔大约12小时的间隔。作为一个例子,一个病人接受50毫克的NUCYNTA®每天四次(200毫克/天)可以转化为100毫克NUCYNTA®呃一天两次。
转换从其他阿片类药物NUCYNTA®
没有建立转换比率转换从其他阿片类NUCYNTA®ER定义的临床试验。停止所有其他阿片药物当NUCYNTA®开始治疗。
虽然有有用的阿片等价物现成的表,有大量inter-patient可变性的相对效力不同的阿片类药物和产品。因此,它更安全低估患者24小时口服tapentadol需求并提供救援药物(如速阿片)比高估了24小时口服tapentadol需求导致不良反应。
总的来说,与其他阿片类止痛药一样,首先估计每日tapentadol要求的一半作为初始剂量,管理与速释救援药物镇痛不足的补充。
转换从美沙酮NUCYNTA®
密切监测尤为重要,从美沙酮转化为其他阿片受体激动剂。美沙酮之间的比例和其他阿片受体激动剂可能相差很大的函数前剂量曝光。美沙酮半衰期很长,可以积累的等离子体。
2.2滴定和维护治疗
分别滴定NUCYNTA®ER提供足够的镇痛的剂量和最大限度地减少不良反应。不断地重新评估患者接受NUCYNTA®ER评估疼痛控制的维护和相关不良反应的发生率,以及监测成瘾的发展,滥用或误用。频繁的开药者之间的沟通是很重要的,医疗保健团队的其他成员,病人和照顾者/家庭期间改变镇痛需求,包括最初的滴定。在长期治疗,定期评估持续阿片类止痛药的必要性。
滴定患者足够的镇痛剂量增加50毫克每日每三天不超过两次。在临床研究中,功效与NUCYNTA®ER证明相对于安慰剂在100毫克到250毫克的剂量范围内每天两次(见临床研究(14))。
突破疼痛的患者可能需要增加剂量的NUCYNTA®,或可能需要救援药物与适当的速释镇痛的剂量。如果剂量稳定后的疼痛程度增加,试图确定的来源增加疼痛之前增加NUCYNTA®ER剂量。
如果不能接受opioid-related不良反应观察,随后的剂量可能会减少。调整剂量以获得一个适当的平衡管理的痛苦和opioid-related不良反应。
2.3中止NUCYNTA®
当病人不再需要治疗NUCYNTA®ER平板电脑,使用逐步下行的滴定剂防止戒断症状和体征的病人。
2.4患者肝损伤
使用NUCYNTA®ER在严重肝损伤患者不推荐(儿童得分10 - 15)。
中度肝损害患者(儿童得分7 - 9),启动治疗使用50毫克NUCYNTA®ER和管理没有比每隔24小时更频繁。对中度肝损伤患者的最大推荐剂量为100毫克的NUCYNTA®每天ER(见临床药理学(12.3))。
不推荐剂量调整患者的轻度肝损害(儿童得分5到6)(见警告和注意事项(5.14)和临床药理学(12.3)]。
2.5患者肾功能损害
不推荐剂量调整患者的轻度或中度肾功能损害。使用NUCYNTA®ER有严重肾功能损害的患者不建议(见警告和注意事项(5.15)和临床药理学(12.3)]。
2.6老年病人
一般来说,推荐剂量老年病人与正常肾和肝脏功能是一样的年轻成人患者与正常肾和肝脏功能。因为老年患者更有可能减少肾和肝脏功能,应该考虑从老年患者较低的推荐剂量范围(见临床药理学(12.3))。
2.7管理NUCYNTA®
指导病人吞咽NUCYNTA®ER平板电脑。平板电脑不被削减,压碎,溶解,或咀嚼由于快速释放和吸收的风险可能致命剂量的tapentadol(见警告和预防措施(5.1,5.2)]。
指导患者采取NUCYNTA®呃一平板电脑时间和足够的水以确保完成吞咽后立即放置在口中(见警告和注意事项(5.2),和患者咨询信息(17)]。
-

妥泰
![Topamax (Topiramate) Tablet, Coated Topamax (Topiramate) Capsule, Coated Pellets [Janssen Pharmaceuticals, Inc.] 妥泰(托吡酯)平板电脑,涂布妥泰(托吡酯)胶囊,涂层颗粒(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=21628112-0c47-11df-95b3-498d55d89593&name=topamax-04.jpg)
2.1癫痫
没有必要监控托吡酯等离子体浓度优化妥泰®(托吡酯)治疗。
有时,妥泰®的添加苯妥英可能需要调整剂量的苯妥英达到最佳的临床结果。添加或撤回苯妥英、卡马西平在辅助治疗治®可能需要调整剂量的妥泰®。
因为苦味,平板电脑不应该被打破。
妥泰®可以不考虑。
单一疗法使用
成人和儿科患者10年及以上
妥泰®的推荐剂量单药治疗成人和儿科患者10岁及以上是在两个分裂的剂量400毫克/天。大约58%的患者随机分配到400毫克/天达到最大剂量单药治疗的对照试验;平均剂量的试验是275毫克/天。应该通过滴定剂量根据以下时间表(表1):
表1:单一疗法滴定时间表成人和儿科患者10年及以上的早上剂量晚上第一周25 mg剂量25 mg 2 50毫克50毫克每周3 75毫克75毫克4 100毫克100毫克每周5 150毫克150毫克星期6 200毫克200毫克2岁儿童< 10年
剂量的托吡酯作为初始单药治疗2到10岁以下儿童部分性或广义tonic-clonic癫痫主要是基于pharmacometric桥接方法(见临床研究(14.1))。
剂量的患者2 < 10年是基于重量。在滴定时期,妥泰®的初始剂量应25毫克/天夜间管理第一周。基于耐受性,剂量可以增加到50毫克/天(25毫克每日两次)在第二个星期。剂量可以增加25 - 50毫克/天每个随后的星期容忍。滴定最低维持剂量应尝试在5 - 7周总滴定的时期。基于耐受性和临床反应,额外的滴定更高剂量(最大维持剂量)可以在25 - 50毫克/天尝试每周增量。每日总剂量不得超过最大维持剂量为每个范围的体重(表2)。
表2:单一疗法的目标总日常维护剂量对患者2 < 10年体重(公斤)每日总剂量(毫克/天)*最低维持剂量每日总剂量(毫克/天)*最大两个同样分剂量维持剂量* 11 150 250 12 - 22 200 300 23 - 31 200 350 32 - 38 250 350 250大于400辅助治疗使用
17岁及以上的成人——部分发作癫痫,主要推广Tonic-Clonic癫痫,或Lennox-Gastaut综合症
推荐的每日总剂量的妥泰®作为辅助治疗成人部分发作癫痫是200到400毫克/天,分两次,和400毫克/天,分两次作为辅助治疗成人原发性广义tonic-clonic发作。建议治疗开始在25到50毫克/天,紧随其后的是滴定的有效剂量增加每周25到50毫克/天。滴定的增量25毫克/天每周可能会推迟时间达成有效剂量。剂量超过400毫克/天(600年、800年或1000毫克/天)没有显示改善反应剂量反应研究成人部分发作癫痫发作。每日剂量1600毫克以上没有被研究过。
主要研究广义tonic-clonic癫痫,最初的滴定率低于先前的研究;分配的剂量达到8周结束时(见临床研究(14.1))。
儿科患者年龄在2 - 16年部分发作癫痫,主要推广Tonic-Clonic癫痫,或Lennox-Gastaut综合症
推荐的每日总剂量的妥泰®作为辅助治疗小儿患者部分性癫痫,主要推广tonic-clonic癫痫,或癫痫发作与Lennox-Gastaut综合征大约是5到9毫克/公斤/天,分两次。滴定应该开始在25毫克/天(或更少,基于一系列的1到3毫克/公斤/天)夜间第一周。用量应该每隔1 -或2周增加了增量1到3毫克/公斤/天(管理,分两次),达到最佳的临床反应。应该遵循临床剂量滴定的结果。beplay体验
主要研究广义tonic-clonic癫痫,最初的滴定率低于先前的研究;分配的剂量的6毫克/公斤/天结束时达成8周(见临床研究(14.1))。
2.2偏头痛
推荐的每日总剂量的妥泰®作为治疗成人和12岁以上的青少年预防偏头痛的两个分裂的剂量100毫克/天(表3)。推荐的滴定率托吡酯对偏头痛预防100毫克/天的方法是:
表3:偏头痛预防滴定时间表12岁及以上成人和青少年患者早晨剂量晚上剂量1没有25 mg 2周25毫克25毫克3 25毫克50毫克每周4 50毫克50毫克剂量和滴定速度应该遵循临床结果。beplay体验如果需要,可以使用剂量调整时间间隔。
妥泰®可以不考虑。
2.3管理妥泰®洒胶囊
妥泰®(托吡酯胶囊)洒胶囊可能吞下全部或可能由仔细打开胶囊,洒少量的全部内容(茶匙)软的食物。这种药物/混合物应立即吞下,而不是咀嚼食物。它不应该被存储,以供将来使用。
2.4患者肾功能损害
在肾功能受损的受试者(肌酐清除率少于70毫升/分钟/ 1.73平方米),一半的成人推荐剂量。这类患者需要长时间在每个剂量达到稳态。
2.5老年患者(65岁以上)
剂量调整可能表示在老年病人受损的肾功能(肌酐清除率< 70 mL / min / 1.73平方米)是显而易见的(见临床药理学(12.3))。
2.6接受血液透析的患者
托吡酯是通过血液透析的速度是4到6倍于一个正常的人。因此,长期的透析可能导致托吡酯浓度低于需要维护一个抗癫痫作用。为了避免托吡酯血浆浓度快速下降在血液透析过程中,可能需要补充剂量的托吡酯。实际的调整应该考虑1)透析的时间期间,2)清除率透析系统的使用,和3)的有效肾清除率托吡酯在病人透析。
2.7患者肝脏疾病
在hepatically受损的患者中,托吡酯等离子体浓度可能会增加。的机制还不是很清楚。
-

Invega
![Invega (Paliperidone) Tablet, Extended Release [Janssen Pharmaceuticals, Inc.] Invega (Paliperidone)平板电脑,延长释放(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=7b8e5b26-b9e4-4704-921b-3c3c0d159916&name=invega-02.jpg)
2.1精神分裂症
成年人
的推荐剂量INVEGA®(paliperidone)延长释放片治疗精神分裂症的成年人是6毫克每日服用一次。初始剂量滴定不是必需的。虽然还没有系统地建立剂量6毫克以上有额外的好处,有一个总体趋势与高剂量更大的影响。这一定是体重增加剂量相关的不良反应。因此,一些患者可能受益于更高的剂量,12毫克/天,和对一些病人来说,较低剂量的3毫克/天可能就足够了。剂量增加6毫克/天以上应该只有在临床评估,通常应该发生在间隔超过5天。当剂量增加表示,增加3毫克/天。的最大推荐剂量是12毫克/天。
在长期的研究中,INVEGA®已被证明是有效的延迟时间复发在精神分裂症患者稳定在INVEGA®6周(见临床研究(14))。INVEGA®应规定维护临床稳定的最低有效剂量和医生应定期重新评估个体患者的药物的长期有效性。
青少年(12 - 17岁)
的推荐起始剂量INVEGA®(paliperidone)延长释放片治疗精神分裂症的12 - 17岁的青少年是3毫克每日服用一次。初始剂量滴定不是必需的。剂量增加,如果认为有必要,应该只有在临床评估,应该发生在增量3毫克/天的间隔超过5天。开处方者应该注意到,在青少年精神分裂症的研究中,没有明确的增强疗效高剂量,即。6毫克的受试者体重不到51公斤,12毫克受试者体重51公斤或更高版本,而剂量相关性不良事件。
2.2分裂情感性障碍
的推荐剂量INVEGA®(paliperidone)延长释放片治疗分裂情感性障碍的成年人是6毫克每日服用一次。初始剂量滴定不是必需的。有些病人可能受益于更低或更高剂量的推荐剂量范围内3 - 12毫克每日一次。总的趋势与高剂量都能看到更大的影响。这一趋势是增加剂量相关的不良反应。剂量调整,如果出现表示,只有在临床评估。剂量增加,如果表示,通常应该发生在间隔超过4天。当剂量增加表示,增加3毫克/天。的最大推荐剂量是12毫克/天。
2.3管理指令
INVEGA®可以有或没有食物。
INVEGA®必须吞下整个的液体。平板电脑不应该咀嚼、分裂或粉碎。药物时是包含在一个外壳设计释放药物以控制速度。平板电脑外壳,不溶性的核心组件,从体内消除;病人不应该担心如果他们偶尔注意到凳子上的东西看起来像一个平板电脑。
2.4使用利培酮
同时使用INVEGA®与利培酮还没有被研究过。由于paliperidone利培酮的主要活性代谢产物,应该考虑添加剂paliperidone暴露如果利培酮coadministered INVEGA®。
2.5特殊人群的剂量
肾功能损害
剂量必须根据病人的个性化肾功能状态。轻度肾功能障碍患者(肌酐清除率≥50 mL / min < 80毫升/分钟),推荐的初始剂量的INVEGA®是3毫克每日一次。剂量可以增加到最多6毫克,每日一次,根据临床反应和耐受性。中度到重度的患者肾功能损害(肌酐清除率≥10 mL / min < 50毫升/分钟),推荐的初始剂量的INVEGA®1.5毫克,每日一次,这可能是增加到最多3毫克每天一次后临床评估。作为INVEGA®尚未研究患者的肌酐清除率低于10毫升/分钟,在这类患者中使用不推荐。(见临床药理学(12.3))
肝损伤
轻度至中度肝损害的患者(儿童分类A和B),没有剂量调整建议(见临床药理学(12.3))。INVEGA®尚未在严重肝损伤患者进行研究。
上了年纪的
因为老年病人肾功能减弱,剂量调整可能需要根据他们的肾功能状态。一般来说,老年人肾功能正常的患者推荐剂量是一样的年轻成人肾功能正常的患者。中度到重度的患者肾功能损害(肌酐清除率10 mL / min < 50毫升/分钟)的最大推荐剂量INVEGA®是3毫克每天一次(见上面肾功能损害)。
-
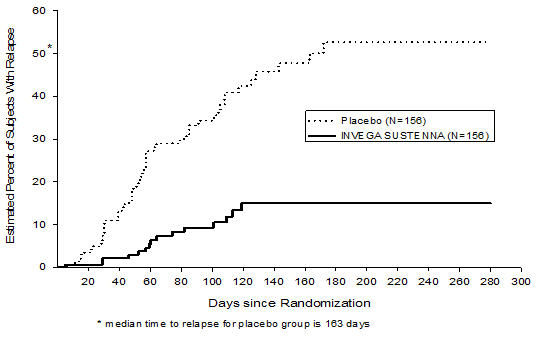
Invega Sustenna
![Invega Sustenna (Paliperidone Palmitate) Injection [Janssen Pharmaceuticals, Inc.] Invega Sustenna (Paliperidone棕榈酸酯)注入(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=1af14e42-951d-414d-8564-5d5fce138554&name=invega-13.jpg)
2.1管理指令
每个注射必须只能由医疗专业管理。
注射用药物的药物产品应该为异物检查视力和变色政府之前,只要产品和容器许可证。
INVEGA SUSTENNA®的目的是仅供肌内使用。不执行任何其他路线。避免无意注入血管。管理一个注射的剂量;不管理分为注射的剂量。慢慢注入,深入肌肉。
推荐的针头大小管理INVEGA SUSTENNA®到三角肌是由病人的体重:
对患者体重小于90公斤,1英寸,23日计针建议。重达90公斤以上,患者1½英寸,建议22计针。三角肌注射应该两个三角肌肌肉之间的交替。
推荐的针头大小管理INVEGA SUSTENNA®的臀部肌肉1½英寸,22计针不管病人的体重。
管理upper-outer象限的臀肌。臀部注射应该两臀部肌肉之间的交替。
2.2精神分裂症和分裂情感性障碍
患者从未口服paliperidone或口服或注射利培酮,建议建立与口服耐受性paliperidone启动之前或口服利培酮治疗INVEGA SUSTENNA®。
为每一个批准的推荐剂量INVEGA SUSTENNA®迹象显示在表1。的推荐起始INVEGA SUSTENNA®234毫克的剂量是治疗第一天和156毫克一周后,在三角肌中取样的;管理。第二起始剂量后,每月维护剂量可以管理在三角肌或臀部肌肉。
表1。推荐剂量的INVEGA SUSTENNA®成人患有精神分裂症和分裂情感性障碍指示起始剂量(三角肌)每月维持剂量*(三角肌或臀)最大月度剂量1天8 * 5周后第一次注射。†治疗精神分裂症的推荐维持剂量为117毫克。有些病人可能受益于更低或更高版本维护剂量内可用的额外优势(39毫克,78毫克,156毫克和234毫克)。‡基于耐受性调整剂量和/或有效性使用可用的优势。39毫克强度不是长期分裂情感性障碍研究的研究。精神分裂症234毫克156毫克39 - 234毫克__ 234毫克分裂情感性障碍234毫克156毫克78 - 234毫克‡234毫克维持剂量的调整可能每月。当进行剂量的调整,prolonged-release特点INVEGA SUSTENNA®应考虑(见临床药理学(12.3)],全效的剂量调整几个月可能不明显。
2.3错过剂量
避免错过剂量
建议第二起始剂量INVEGA SUSTENNA®是一个星期后第一个剂量。为了避免错过剂量,患者可以第二次剂量4天之前或之后一周的时间点。同样,第三和随后注射后启动方案建议每月。为了避免错过了每月的剂量,患者可以注射7天之前或之后每个月的时间点。
错过了第二起始剂量的管理
如果目标日期第二INVEGA SUSTENNA®注入(一周±4天)是错过了,建议重新启动取决于的时间运行以来病人的注射。对于错过第二起始剂量按照表2中提供的剂量指示。
表2。管理错过第二起始剂量的时机错过了第二起始剂量剂量少于4周以来第一次注射管理第二起始剂量156毫克的三角肌肌肉尽快。建议管理第三注入117毫克臀大肌三角肌或第一次注射后5周(不管第二次注射的时间)。此后,在三角肌或恢复常规月度计量臀部肌肉。4 - 7周以来第一次注射的简历与两个注射剂量156毫克以下方式:管理尽快三角肌注射。管理一个三角肌注射后1周。此后,在三角肌或恢复常规月度计量臀部肌肉。7周多以来第一次注射重启与推荐起始剂量(参见2.2节,表1):管理一个234毫克三角肌注射1天。管理156毫克三角肌注射1星期后。此后,在三角肌或恢复常规月度计量臀部肌肉。管理一个错过了维持剂量
对于错过的维持剂量按照计量表3提供的指导。
表3。管理错过时机错过了维持剂量的维护自去年注射剂量给药4到6周恢复定期每月计量尽快之前稳定的病人的剂量,紧随其后的是注射在每月的间隔。超过6周,6个月自去年注射的简历相同剂量的病人以前稳定(除非病人稳定在234毫克的剂量,然后第一个2注射应该每156毫克)在以下方式:管理尽快三角肌注射。管理一个三角肌注射1星期后在同一剂量。此后,简历管理之前稳定剂量的三角肌或臀部肌肉第二次注射后1个月。超过6个月,自去年注射重启与推荐起始剂量(参见2.2节,表1):管理一个234毫克三角肌注射1天。管理156毫克三角肌注射1星期后。此后,简历管理之前稳定剂量的三角肌或臀部肌肉第二次注射后1个月。2.4使用利培酮或口服Paliperidone
由于paliperidone利培酮的主要活性代谢产物,应该小心谨慎当INVEGA SUSTENNA®是coadministered与利培酮或口服paliperidone长时间。安全数据涉及伴随使用INVEGA SUSTENNA®和其他抗精神病药物是有限的。
2.5剂量调整
肾功能损害
INVEGA SUSTENNA®尚未系统研究患者的肾功能损害(见临床药理学(12.3))。轻度肾功能障碍患者(肌酐清除率≥50 mL / min < 80毫升/分钟(Cockcroft-Gault公式)),启动INVEGA SUSTENNA®156毫克剂量的治疗一天1和117毫克一周后。管理两个剂量在三角肌中取样。之后,按照每月注射78毫克的三角肌或臀部肌肉(参见特定人群的使用(8.6)和临床药理学(12.3)]。
INVEGA SUSTENNA®不推荐患者中度或重度肾功能损害(肌酐清除率< 50毫升/分钟)(见使用在特定人群(8.6)和临床药理学(12.3)]。
共同拥有强大CYP3A4 / 22 (P-gp)诱导物
可能需要增加剂量的INVEGA SUSTENNA®当强烈的CYP3A4和P-gp诱导物(如卡马西平、利福平、圣约翰草)是流行性流感减毒活疫苗。相反,在强烈的诱导物,停药可能需要减少剂量的INVEGA SUSTENNA®(见药物相互作用(7.2)和临床药理学(12.3)]。
2.6从其他抗精神病药物
没有系统地收集数据具体地址转换病人患有精神分裂症和分裂情感性障碍与其他抗精神病药物INVEGA SUSTENNA®,或关于伴随管理与其他抗精神病药物。
2.6.1从口服抗精神病药物
的患者从未口服paliperidone或口服或注射利培酮,应该建立耐受性口服paliperidone或口服利培酮在开始治疗之前INVEGA SUSTENNA®。
前口服抗精神病药物可以逐渐停止的时候开始治疗INVEGA SUSTENNA®。建议启动INVEGA SUSTENNA®234毫克的剂量是治疗第一天和156毫克一周后,两个管理在三角肌中取样的;(见剂量和管理(2.2))。病人以前稳定在不同剂量的INVEGA®延长释放平板电脑可以获得类似paliperidone稳态维持治疗期间接触INVEGA SUSTENNA®每月剂量如表4中所示。
表4。剂量的INVEGA®和INVEGA SUSTENNA®需要达到类似的稳态paliperidone暴露在维持治疗期间制定INVEGA®延长释放平板INVEGA SUSTENNA®注射给药频率每天一次每隔4周剂量(mg) 1263 23411739 - 782.6.2从长效注射抗精神病药物
的患者从未口服paliperidone或口服或注射利培酮,应该建立耐受性口服paliperidone或口服利培酮在开始治疗之前INVEGA SUSTENNA®。
切换时患者目前稳态长效注射抗精神病,启动INVEGA SUSTENNA®疗法的下一个计划注入。INVEGA SUSTENNA®应该继续在每月的间隔。2.2节中描述的一周的开始给药方案不是必需的。参见表1上面推荐的月度维护剂量。根据以往的临床耐受性和/或有效性的历史,一些患者可能受益于更低或更高版本维护剂量内可用的优势(39毫克,78毫克,117毫克,156毫克和234毫克)。39毫克强度不是长期分裂情感性障碍研究的研究。每月维护剂量可以在三角肌或臀部肌肉注射(见剂量和管理(2.2))。
如果INVEGA SUSTENNA®是中断,必须考虑其prolonged-release特征。与其他抗精神病药物推荐,需要继续现有的锥体外系症状(EPS)药物应该定期重新评估。
2.7说明使用
每个注射必须只能由医疗专业管理。
套件包含一个肾上腺素注射器和2安全针(1½英寸22计针和一个1英寸23计针)肌内注射。
INVEGA SUSTENNA®是仅供单使用。
。奶昔注射器大力至少10秒,以确保均匀悬浮。b。选择适当的针。三角肌注射:
如果病人体重不超过90公斤,使用1英寸23日计针(针和蓝颜色的中心)。如果病人重达90公斤以上,使用1½英寸22计针(针和灰色有色中心)。臀部注射:
使用1½英寸22计针(针和灰色有色中心)不管病人的体重。
c。虽然拿着注射器直立,去掉橡胶尖帽容易顺时针扭转运动。d。皮安全针袋一半开放。掌握使用塑料皮袋针鞘。附加的安全针的鲁尔接口连接注射器与一个简单的顺时针扭转运动。e。把针鞘远离直拔针。不扭曲鞘从注射器针可能放松。f。带来附加的注射器针de-aerate在直立位置。De-aerate注射器的柱塞杆小心翼翼地向前移动。g。慢慢注入肌肉内的整个内容,深入所选择的病人的三角肌或臀部肌肉。不执行任何其他路线。 h. After the injection is complete, use either thumb or finger of one hand (h1, h2) or a flat surface (h3) to activate the needle protection system. The needle protection system is fully activated when a 'click' is heard. Discard the syringe with needle appropriately. h1 h2 h3 -

利培酮
![Risperdal (Risperidone) Tablet Risperdal M-tab (Risperidone) Tablet, Orally Disintegrating Risperdal (Risperidone) Solution [Janssen Pharmaceuticals, Inc.] 利培酮(利培酮)片利培酮M-tab(利培酮)片,口服瓦解利培酮(利培酮)解决方案(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=7e117c7e-02fc-4343-92a1-230061dfc5e0&name=risperdal-07.jpg)
表1。每日推荐剂量的初始剂量滴定法指示(增量)精神分裂症目标剂量有效剂量范围:成年人(2.1)2毫克1 - 2毫克4到8毫克4到16毫克精神分裂症:青少年(2.2)0.5 0.5毫克1毫克3毫克1到6毫克双相躁狂:成年人(2.2)2 - 3毫克1毫克1到6毫克1到6毫克双相躁狂:孩子andadolescents(2.2) 0.5 0.5毫克1毫克1到2.5毫克1到6毫克易怒自闭症(2.3)0.25 mgCan to0.5毫克增加第四天:(体重少于20公斤)0.5 mgCan to1毫克增加第四天:(体重大于或等于20公斤)后第四天,每隔> 2周:0.25毫克(体重少于20公斤)0.5毫克(体重大于或等于20公斤):0.5毫克(体重少于20公斤):1毫克(体重大于或等于20公斤)0.5到3毫克
严重的肾和肝损伤在成人:使用低剂量的0.5毫克,每日两次。可能会增加剂量高于1.5毫克,每日两次,每隔一个星期或更长时间。
2.1精神分裂症
成年人
通常初始剂量
利培酮®可以每天服用一次或两次。初始剂量是2毫克/天。可能会增加剂量或更高版本,每隔24小时在每天增加1 - 2毫克,容忍,推荐剂量的每天4到8毫克。在一些病人,缓慢滴定可能是适当的。功效已经证明在一系列4毫克每天16毫克。然而,剂量6毫克/天以上每天两次剂量不证明比低剂量更有效,与更多的锥体外系症状和其他有关不良反应,一般不推荐。在一个研究支持每日一次给药,疗效结果8毫克普遍强于4毫克。每天的安全剂量高于16毫克尚未评估在临床试验中(见临床研究(14.1))。
青少年
初始剂量为0.5毫克,每日一次,管理作为一个单日剂量在早上或晚上。剂量可能调整每隔24小时或更高版本,增加0.5毫克或1毫克/天,容忍,推荐剂量的3毫克/天。虽然功效的研究已经证明了青少年精神分裂症患者在1毫克剂量6毫克/天,没有额外的好处每天观察3毫克以上,和高剂量相关的不良事件。剂量高于6毫克每天并没有被研究过。
病人经历持续嗜睡可能受益于管理每天两次剂量的一半。
维持治疗
虽然是未知的精神分裂症患者应该保持多久利培酮®,利培酮的有效性®2毫克每天8毫克/天延迟复发在一个对照试验证明在成年病人临床稳定至少4周,随后一段时间的1到2年(见临床研究(14.1))。两个成人和青少年患者反应敏锐地一般应保持在有效剂量超出了急性发作。病人应定期重新评估,以确定需要维持治疗。
重新启动之前停止治疗的病人
尽管没有数据具体地址重新启动治疗,建议间隔后利培酮®,最初的滴定安排应遵循。
从其他抗精神病药物
没有系统地收集数据具体地址转换精神分裂症患者与其他抗精神病药物利培酮®,或伴随患者抗精神病药物。
2.2双相躁狂
常规剂量
成年人
最初的剂量范围是2毫克到3毫克/天。剂量可能调整每隔24小时或更高版本,1毫克/天的增量。有效剂量范围是1毫克到6毫克/天,在短期内学习,安慰剂对照试验。在这些试验中,短期(3周)anti-manic功效是在一个灵活的剂量范围1毫克到6毫克/天(见临床研究(14.2,14.3)]。利培酮®剂量高于6毫克每天没有研究。
儿科
初始剂量为0.5毫克,每日一次,管理作为一个单日剂量在早上或晚上。剂量可能调整每隔24小时或更高版本,增加0.5毫克或1毫克/天,容忍,推荐的目标剂量的1毫克每天2.5毫克。虽然功效研究已经证明了儿科双相躁狂患者的剂量每天0.5毫克和6毫克之间,没有额外的好处上面观察每天2.5毫克,和高剂量相关的不良事件。剂量高于6毫克每天并没有被研究过。
病人经历持续嗜睡可能受益于管理每天两次剂量的一半。
维持治疗
没有证据可以从对照试验指导临床医生在病人的长期管理改善与利培酮治疗急性躁狂发作期间®。beplay体验虽然普遍认为,药物治疗急性反应之外的躁狂是可取的,为维护的最初反应和预防新躁狂发作,没有系统地获得数据支持使用利培酮®(即在这种长期的治疗。除了3周)。医生选择使用利培酮®长时间应定期重新评估药物的长期风险和好处为个别病人。
2.3易怒与自闭症有关——儿科(儿童和青少年)
利培酮®的用量应根据响应和个性化的病人的耐受性。每日总剂量的利培酮®可以每日服用一次,或每日总剂量的一半可以每天服用两次。
患者体重小于20公斤,每天开始剂量为0.25毫克。患者体重大于或等于20公斤,每天开始剂量为0.5毫克。至少四天之后,推荐剂量的剂量可能会增加到0.5毫克每天病人少于20公斤和1.0毫克每天病人大于或等于20公斤。保持这个剂量至少14天。没有达到足够的临床反应,患者剂量可能会增加每隔2周或更高版本,增量每天0.25毫克的患者不到20公斤,或增加0.5毫克每天病人大于或等于20公斤。有效剂量范围是3毫克/天0.5毫克。没有定量的数据可用于儿童体重小于15公斤。
一旦获得并维持足够的临床反应,考虑逐步降低剂量达到最佳平衡的疗效和安全性。医生选择使用利培酮®长时间应定期重新评估药物的长期风险和好处为个别病人。
病人经历持续嗜睡可能受益于每日一剂量每天睡前或管理一半的剂量每天两次,或减少剂量。
2.4严重肾或肝损伤患者的剂量
严重肾功能损害患者(CLcr < 30 mL / min)或肝损伤(10 - 15点孩子普系统),最初的起始剂量为0.5毫克,每日两次。增量的剂量可能增加0.5毫克,每天服用两次。增加剂量高于1.5毫克,每日两次,间隔一个星期或更多(参见使用在特定人群(8.6和8.7)]。
2.5剂量调整特定的药物相互作用
当利培酮®流行性流感减毒活疫苗与酶诱导物(如卡马西平)的剂量利培酮®应该增加了病人的常规剂量的两倍。可能需要减少利培酮®剂量酶诱导物如卡马西平停止时(见药物相互作用(7.1))。类似的效果可能会与利培酮合并施打®和其他酶诱导物(如苯妥英、利福平、苯巴比妥)。
当氟西汀、帕罗西汀与利培酮®流行性流感减毒活疫苗,利培酮®的剂量应减少。利培酮®剂量不得超过8毫克每天在成人流行性流感减毒活疫苗与这些药物。初始治疗时,利培酮®应该缓慢滴定。可能需要增加剂量利培酮®酶抑制剂如氟西汀、帕罗西汀停止时(见药物相互作用(7.1))。
2.6管理利培酮®口服液
利培酮®口服溶液可直接从校准吸管接种,或可以混合饮料之前管理。利培酮®口头解决方案兼容以下饮料:水,咖啡,橙汁,和低脂牛奶;不兼容可乐或茶。
2.7使用说明利培酮®M-TAB®口腔崩解片
平板电脑访问
利培酮®M-TAB®口腔崩解片0.5毫克,1毫克,2毫克
利培酮®M-TAB®口腔崩解片0.5毫克,1毫克,2毫克泡包中提供的4片。
不要打开泡直到准备好管理。针对单一平板电脑删除,独立的四个水泡的单位在穿孔撕裂。弯曲的角落。皮箔暴露平板电脑。不通过箔推动平板电脑,因为这可能损害平板电脑。
利培酮®M-TAB®口腔崩解片3毫克和4毫克
利培酮®M-TAB®口腔崩解片3毫克和4毫克提供在一个儿童安全袋包含一个水泡1片。
儿童安全袋应该被打开缺口访问水泡。不要打开泡直到准备好管理。皮从侧面烘托暴露平板电脑。不要把平板电脑通过箔,因为这可能损害平板电脑。
平板电脑管理
使用干燥的手,把平板电脑从泡单位,并立即把整个利培酮®M-TAB®口头瓦解平板在舌头上。口头的利培酮®M-TAB®瓦解平板应立即使用,随着平板电脑不能远离泡单元存储一次。利培酮®M-TAB®口腔崩解片分解口腔内秒,随后可以吞下有或没有液体。病人不应该试图分裂或咀嚼片。
-

利培酮Consta
![Risperdal Consta (Risperidone) Kit [Janssen Pharmaceuticals, Inc.] 利培酮Consta(利培酮)工具包(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=bb34ee82-d2c2-43b8-ba21-2825c0954691&name=risperdal-28.jpg)
的患者从未口服利培酮®,建议建立耐受性口服利培酮®开始治疗前与利培酮CONSTA®。
利培酮CONSTA®应每两周由深肌内(IM)三角肌和臀注入。每个注射应该由医疗专业使用适当的封闭安全针(见剂量和管理(2.8))。三角肌管理,使用1英寸针交替注射在两臂之间。臀肌的管理,使用2英寸针交替注入两臀部。不管理静脉注射。
2.1精神分裂症
治疗精神分裂症的推荐剂量为25毫克IM每2周。尽管剂量反应的有效性尚未建立了利培酮CONSTA®,有些病人没有反应到25毫克可能受益于高剂量为37.5毫克,50毫克。最大剂量不得超过50毫克利培酮CONSTA®每2周。没有观察到额外的好处与剂量大于50毫克利培酮CONSTA®;然而,观察不良反应的发生率较高。
利培酮的疗效CONSTA®治疗精神分裂症尚未评估在控制临床试验超过12周。虽然控制研究尚未回答的问题多长时间服用利培酮治疗的精神分裂症患者应该CONSTA®,口服利培酮已被证明是有效的延迟时间复发在长期使用。建议患者继续回应与利培酮治疗CONSTA®所需的最低剂量。医生选择使用利培酮CONSTA®长时间应定期重新评估药物的长期风险和好处为个别病人。
2.2双相情感障碍
的推荐剂量单药治疗或辅助治疗锂或丙戊酸钠的维持治疗双相I型是25毫克IM每2周。有些病人可能受益于高剂量为37.5毫克,50毫克。剂量高于50毫克人口尚未研究。医生选择使用利培酮CONSTA®长时间应定期重新评估药物的长期风险和好处为个别病人。
2.3通用计量信息
较低的初始剂量的12.5毫克保证剂量调整时可能会适当的临床因素,如患者的肝或肾功能损害,对某些药物的相互作用,增加利培酮的血浆浓度(见药物相互作用(7.11))或在患者精神药物耐受性差的历史。12.5毫克剂量的疗效尚未进行临床试验。
口服利培酮®(或其他抗精神病药物)应与第一注射利培酮CONSTA®,持续了3周(然后停止),以确保足够的治疗前血浆浓度保持主要发布阶段的利培酮注射部位(见临床药理学(12.3))。
经常向上调整剂量不应超过每4周。的临床疗效剂量调整不应预期提前3周后第一次注射高剂量。
患者的肝或肾功能损害等临床因素或某些药物的相互作用,增加利培酮的血浆浓度(见药物相互作用(7.11)),减少低至12.5毫克剂量可能是合适的。12.5毫克剂量的疗效尚未进行临床试验。
不要将两种不同剂量的长处的利培酮CONSTA®在一个单一的管理。
2.4特殊人群的剂量
上了年纪的
为老年患者利培酮CONSTA®,推荐剂量为25毫克IM每2周。口服利培酮®(或其他抗精神病药物)应与第一注射利培酮CONSTA®,应该持续3周,以确保合适的治疗前血浆浓度保持主要发布阶段的利培酮注射部位(见临床药理学(12.3))。
肾或肝损伤
肾或肝损伤患者应该接受滴定剂量的口服利培酮®开始治疗前与利培酮CONSTA®。推荐起始剂量为0.5毫克口服利培酮®第一周期间每天两次,可以增加到1毫克每日两次或2毫克每天一次在第二周。如果每日总剂量的至少2毫克口服利培酮®是耐受性良好,注射25毫克利培酮CONSTA®可以管理每2周。口服补充应该持续了3周,在第一次注射后,直到利培酮的主要释放从注射部位已经开始。在一些病人,缓慢滴定可能是医学上合适的。另外,利培酮的起始剂量CONSTA®12.5毫克可能是合适的。12.5毫克剂量的疗效尚未进行临床试验。
肾功能损害患者消除利培酮的能力可能低于正常的成年人。患者肝脏功能受损可能增加免费的利培酮,可能导致一个增强的效果(见临床药理学(12.3))。老年患者和患者体质低血压患者反应或为谁这样的反应构成特定的风险应该指示nonpharmacologic干预有助于减少直立性低血压的发生(例如,坐在床边几分钟之前试图站在早上,慢慢地从一个坐着的位置)。这些患者应该避免钠损耗或脱水,情况加重低血压(饮酒、高环境温度等)。监测直立的生命体征应考虑(见警告和注意事项(5.7))。
2.5重新启动之前停止治疗的病人
没有数据,具体地址重新启动治疗。当重启病人有一个时间间隔与利培酮治疗CONSTA®,补充口服利培酮®(或其他抗精神病药物)应该管理。
2.6从其他抗精神病药物
没有系统地收集数据具体地址转换病人与其他抗精神病药物利培酮CONSTA®,或关于伴随管理与其他抗精神病药物。以前的抗精神病药物应该持续了3周,在第一次注射后的利培酮CONSTA®,以确保治疗浓度的主要释放阶段将保持到利培酮的注射部位已经开始(见临床药理学(12.3))。的患者从未口服利培酮®,建议建立耐受性口服利培酮®开始治疗前与利培酮CONSTA®。与其他抗精神病药物推荐,需要继续现有的EPS药物应该定期重新评估。
2.7合并施打利培酮CONSTA®和其他某些药物
合并施打卡马西平和其他CYP 3 a4酶诱导物(如苯妥英、利福平、苯巴比妥)与利培酮会导致降低血浆浓度的利培酮和9-hydroxyrisperidone加起来的总和,这可能导致疗效降低利培酮CONSTA®治疗。利培酮需要相应的滴定剂量的患者接受这些酶诱导物,尤其是在启动或停止治疗与这些诱导物(见药物相互作用(7.11))。与卡马西平治疗的起始或其他已知CYP 3 a4肝酶诱导物,应密切监测患者第一次4 - 8周,自利培酮剂量CONSTA®可能需要调整。增加剂量,或额外的口服利培酮®,可能需要考虑。在停药卡马西平或其他CYP 3 a4肝酶诱导物,利培酮的用量CONSTA®应该重新评估,如果有必要,降低了。患者可能放置在较低剂量的利培酮CONSTA®2至4周计划中止前卡马西平或其他CYP 3 a4调整预期增加等离子体浓度的利培酮+ 9-hydroxyrisperidone。推荐剂量的患者25毫克利培酮CONSTA®和中断卡马西平或其他CYP3A4酶诱导物,建议继续治疗25毫克剂量除非临床判断需要降低利培酮CONSTA®剂量12.5毫克或需要中断利培酮CONSTA®治疗。12.5毫克剂量的疗效尚未进行临床试验。
氟西汀、帕罗西汀、CYP 2 d6抑制剂已被证明增加利培酮的血浆浓度分别为2.5 - -2.8倍和3 - 9折。氟西汀并不影响9-hydroxyrisperidone的血浆浓度。帕罗西汀9-hydroxyrisperidone的浓度下降了约10%。利培酮剂量的氟西汀、帕罗西汀时需要相应的滴定流行性流感减毒活疫苗。伴随氟西汀、帕罗西汀启动或停止时,医生应该重新评估剂量的利培酮CONSTA®。氟西汀、帕罗西汀是初始化时,患者可能放置在较低剂量的利培酮CONSTA®2至4周计划开始之前的氟西汀、帕罗西汀治疗调整预期利培酮的血浆浓度的增加。当氟西汀、帕罗西汀发起推荐剂量的患者接受25毫克利培酮CONSTA®,建议继续治疗25 mg剂量除非临床判断需要降低利培酮CONSTA®剂量12.5毫克或需要中断利培酮CONSTA®治疗。当利培酮CONSTA®发起的病人已经接受氟西汀、帕罗西汀,起始剂量为12.5毫克可以考虑。12.5毫克剂量的疗效尚未进行临床试验。中断的影响伴随氟西汀、帕罗西汀治疗利培酮的药物动力学和9-hydroxyrisperidone尚未研究。 [see Drug Interactions (7.11)]
2.8说明使用
重要的信息
利培酮CONSTA®需要密切关注这些使用循序渐进的指示,以确保成功的管理。
使用组件提供
组件在这个剂量包是专门为使用利培酮CONSTA®。利培酮CONSTA®必须重组只提供稀释剂的剂量包装。
不替代任何剂量包装的组件。
不存储调整后悬架吗
管理剂量后尽快调整,避免结算。
适当的剂量
瓶必须管理的全部内容,确保预定剂量的利培酮CONSTA®。
一次性设备
不重用。医疗设备需要特定材料特点如期执行。这些特征已经验证了单只使用。任何试图处理文档的设备后续重用可能影响设备的完整性或导致性能恶化。
剂量包装内容
步骤1装配组件取出剂量包装瓶适配器连接到瓶 等待30分钟剂量包从冰箱里拿出,让坐在室温重组前至少30分钟。不温暖的任何其他方式。除去瓶帽抛掉颜色的瓶帽。擦的灰色塞用酒精擦洗。允许空气干燥。不删除灰色橡胶塞。准备瓶适配器保持无菌水泡如图所示。皮去除衬纸。不要把药瓶适配器从水泡。请勿触摸提示在任何时候。这将导致污染。瓶适配器连接到瓶瓶放置在一个坚硬的表面和持有的基础。中心瓶灰色橡皮塞适配器。 Push vial adapter straight down onto vial top until it snaps securely into place.Do not place vial adapter on at an angle or diluent may leak upon transfer to the vial.肾上腺素注射器连接到瓶适配器 去除消毒水泡保持瓶垂直,防止泄漏。持有的瓶,打开无菌泡去除。不动摇。请勿触摸暴露鲁尔接口开瓶适配器。这将导致污染。使用适当的控制保存的白领的注射器。不要在大会举行玻璃注射器的筒。把帽子拿着白领,提前白色cap.Do不扭曲或切断了白色cap.Do不能碰注射器小费。这将导致污染。切帽可以丢弃。注射器连接到瓶适配器持有瓶适配器的裙子保持静止。保持注射器由白领然后提示插入瓶的鲁尔接口打开适配器。不要把玻璃注射器桶。这可能导致白领放松或分离。把注射器瓶适配器与公司顺时针扭转运动,直到感觉舒适的。不要过度收紧政策。过度紧缩可能导致注射器提示打破。步骤2重新构建微球 整个的稀释剂稀释剂注入注射器注入瓶。暂停在稀释剂微球继续按住柱塞杆,摇晃至少10秒,如图所示。检查悬架。适当混合时,悬架出现统一的,厚,乳白色的颜色。微球在液体中可见。立即进行下一步所以暂停不安定。暂停转移到注射器完全反转瓶。慢慢地把柱塞杆拉到从瓶到注射器支取全部内容。移除瓶适配器持有白领的注射器和旋开瓶适配器。在穿孔撕裂部分的瓶标签。分离标签应用于注射器进行身份鉴定。适当地摒弃两瓶,瓶适配器。第三步把针 选择合适的针选择基于注射针位置(臀部或三角肌)。把针皮泡袋开放部分,用掌握的针,如图所示。拿着白领注射器,把注射器针头鲁尔接口连接与一个公司顺时针扭转运动到舒适的。请勿触摸针鲁尔接口开放。这将导致污染。Resuspend微球完全移除气泡袋。在注射之前,再次剧烈摇动注射器,像一些解决将会发生。第四步注入剂量 删除透明护针移动安全装置回针注射器,如图所示。然后持有白领注射器,小心翼翼地把透明护针直off.Do不是麻花透明针保护器,鲁尔接口连接可能放松。移除气泡针直立和自来水轻轻做出任何气泡上升到顶部。慢慢地小心地按柱塞杆向上去除空气。注射器肌内注射立即注入全部内容(IM)到臀部或病人的三角肌。臀部注射应该制成upper-outer象限的臀部。不管理静脉注射。安全安全装置使用一只手针,针安全装置在一个45度角,平坦的表面。针压公司,快速动作,直到完全从事安全装置。避免针刺损伤:不要使用两只手。不要故意松开或虐待针安全装置。不要试图把针或安全装置如果针弯曲或损坏。如何处置针头针检查确认安全装置是完全参与。丢弃在一个批准的专家容器。也丢弃未使用的针剂量提供的包。 -

昊图公司三Cyclen瞧
![Ortho Tri Cyclen Lo (Norgestimate And Ethinyl Estradiol) Kit [Janssen Pharmaceuticals, Inc.] 昊图公司三Cyclen罗(Norgestimate和乙炔雌二醇)工具包(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=a1cfdb57-58fd-4fbd-ae18-571c97bff2cd&name=ortho-tri-cyclen-25.jpg)
2.1如何开始昊图公司TRI-CYCLEN瞧
昊图公司TRI-CYCLEN Lo在DIALPAK平板电脑自动售货机或分发VERIDATE平板电脑自动售货机(参见如何提供/存储和处理(16)]。昊图公司TRI-CYCLEN Lo可能开始使用第一天开始或周日开始(见表1)。第一个周期的周日开始养生法,应该使用一个额外的避孕方法,直到第一个连续7天的管理。
2.2如何昊图公司TRI-CYCLEN瞧
表1:说明政府正的TRI-CYCLEN Lo完成指令来促进患者咨询适当的平板电脑上使用位于fda批准的病人标识。女性开始COCs目前未使用激素避孕(第一天开始或星期天开始)重要:考虑排卵的可能性和概念开始之前这种产品。平板电脑颜色:正的TRI-CYCLEN Lo活跃的平板电脑是白色的(每天1 - 7),浅蓝色(每天8 - 15)和深蓝色(每天16 - 21)。昊图公司TRI - CYCLEN瞧不活跃的平板电脑是深绿色(每天22到28)。第一天开始:第一次活动平板不考虑膳食在月经的第一天。同时采取后续活动平板电脑一旦每日每天总共21天。每天取一个深绿色不活跃的平板电脑7天,同时,活跃的平板电脑。开始一周的每个后续包在同一天第一周期包(即。当天,在最后一个不活跃的平板电脑)周日开始:采取第一个主动平板不考虑吃饭在月经开始后的第一个星期日。由于怀孕的潜在风险,使用额外的无激素避孕方法(如避孕套和杀精剂)的前七天病人的第一个周期群正的TRI-CYCLEN瞧。同时采取后续活动平板电脑一旦每日每天总共21天。 Take one dark green inactive tablet daily for the following 7 days and at the same time of day that active tablets were taken. Begin each subsequent pack on the same day of the week as the first cycle pack (i.e., on the Sunday after taking the last inactive tablet) and additional non-hormonal contraceptive is not needed. Switching to ORTHO TRI-CYCLEN Lo from another oral contraceptive Start on the same day that a new pack of the previous oral contraceptive would have started. Switching from another contraceptive method to ORTHO TRI-CYCLEN Lo Start ORTHO TRI-CYCLEN Lo: Transdermal patch On the day when next application would have been scheduled Vaginal ring On the day when next insertion would have been scheduled Injection On the day when next injection would have been scheduled Intrauterine contraceptive On the day of removal If the IUD is not removed on first day of the patient's menstrual cycle, additional non-hormonal contraceptive (such as condoms and spermicide) is needed for the first seven days of the first cycle pack. Implant On the day of removal昊图公司开始TRI-CYCLEN Lo堕胎后或流产
对于妊娠前三个月
孕早期流产后或流产,邻位的TRI-CYCLEN罗可能会立即开始。不需要额外的方法避孕,如果正的TRI-CYCLEN Lo立即启动。如果正的TRI-CYCLEN瞧不是开始后5天内终止妊娠,病人应该使用额外的无激素避孕方法(如避孕套和杀精剂)的前七天她第一次循环群正的TRI-CYCLEN瞧。中期妊娠
才开始后4周中期妊娠流产或流产,由于血栓栓塞疾病的风险增加。指令后开始昊图公司TRI-CYCLEN瞧,表1中第一天或者周日开始,。如果使用周日开始,使用额外的无激素避孕方法(如避孕套和杀精剂)的前七天病人的第一个周期群正的TRI-CYCLEN瞧。(见禁忌症(4)、警告和注意事项(5.1),和fda批准的病人标签。)在分娩后开始昊图公司TRI-CYCLEN瞧
才开始后4周交货,由于血栓栓塞疾病的风险增加。后开始避孕治疗与邻位的TRI-CYCLEN Lo指令表1中对女性没有使用激素避孕。昊图公司TRI-CYCLEN瞧不推荐哺乳期妇女使用(见使用在特定的人群(8.3))。如果女人没有一个产后时期,考虑排卵的可能性和观念发生之前使用邻位的TRI-CYCLEN瞧。(见禁忌症(4)、警告和注意事项(5.1),使用特定的人群(8.1和8.3),和fda批准的病人标识)。DIALPAK®平板电脑自动售货机:
设置一天:□第一天开始:打开拨空DIALPAK直到箭头指向的第一天,病人的时期。□周日开始:空DIALPAK上的箭头应指向苏(周日)。插入新添排队添上的“V”形和“V”形的顶部DIALPAK。快速补充。丸“1”准备。总是开始与丸丸循环“1”所示内填满环的一部分。删除药丸通过压低服用避孕药的“1”。避孕药会通过一个洞DIALPAK的后面。病人应该等待24小时下药丸。把药丸”2、“打开拨号DIALPAK第二天在顺时针方向。继续采取每天一片,直到所有的药片了。把拨号避孕药“1”位置把空填满,插入一个新的补充。总是会第一个药丸在每个加了当天的星期,无论当病人的下一时期开始。VERIDATE®平板电脑自动售货机
地方的补充VERIDATE平板电脑分发器,以便补充V缺口是顶部的分配器。按补充下适合坚定下所有的大人物(见下面的例子)。周日如果病人开始服药,应采取第一个活跃的药丸的患者的月经期后的第一个星期日开始。删除第一个活跃的药丸顶部的分配器(周日)按避孕药通过分发器的底部的洞。如果病人将开始服药一天除了周日,日历标签提供了,应该放在日历VERIDATE的中心。将正确的标签,确定正确的开始一天,找到那一天印在蓝色的标签上,并当天第一个白色药片直属V缺口顶部的分配器。删除标签的支持。新闻中心的标签在印刷日历的中心。去除白色药片按避孕药通过分发器的底部的洞。已经采取了所有的深绿色药片后,插入一个新的补充到VERIDATE。 The patient should take the first pill on the next day, even if the patient's period is not over yet.插入新的补充:
电梯的空填满VERIDATE平板分发器。插入新的补充,补充的V形切口顶部的分配器。按补充下适合坚定地大人物。2.3没有平板电脑
表2:说明了邻位的TRI-CYCLEN Lo平板电脑如果一活跃的平板电脑是错过了周1,2,或者3平板电脑尽快。继续每天服用一片,直到包完成。如果两个活跃的平板电脑是错过了周1或2花两个星期错过了平板电脑尽快第二天和接下来的两个活跃的平板电脑。继续每天服用一片,直到包完成。额外的无激素避孕方法(如避孕套和杀精剂)应该作为备用后7天内如果病人性缺失的平板电脑。如果两个活动平板电脑是错过了在第三周或三个或更多活跃的平板电脑连续错过了周1,2或3天1开始:扔掉其余的包,并开始一个新的包。周日开始:继续每天服用一片,直到周日,然后扔掉其余的包,并开始一个新的包。额外的无激素避孕方法(如避孕套和杀精剂)应该作为备用后7天内如果病人性缺失的平板电脑。2.4建议肠胃紊乱
在严重的呕吐或腹泻的情况下,吸收可能不完整的和额外的应采取避孕措施。如果发生呕吐或腹泻后3 - 4小时内采取积极的平板电脑,处理这个问题作为一个错过了平板电脑(参见fda批准的病人标识)。
-

将头发再生治疗的女性
![Equate Hair Regrowth Treatment For Women (Minoxidil) Solution [Wal-mart Stores Inc] 将头发再生治疗女性(米诺地尔)解决方案(沃尔玛)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=e921054f-b3f1-4624-8edd-f6628c6f0fd9&name=nucynta-13.jpg)
NUCYNTA®口头解决方案可用在一个浓度:20毫克/毫升。
照顾当处方和管理NUCYNTA®口头解决避免剂量错误,这可能导致意外过量和死亡。照顾,以确保适当的剂量是沟通和分发。包括毫升(毫升)和毫克剂量(mg)在写药方。时总是使用封闭式校准口腔注射器管理NUCYNTA®口服溶液,确保准确剂量测量和管理。
2.1个性化的剂量
与任何阿片类药物产品,单独为每个病人调整给药方案,考虑到病人的镇痛治疗经验。在tapentadol初始剂量的选择,注意以下几点:
每日总剂量,阿片类药物的效力和具体特征患者已经服用之前;相对效力的可靠性估计所需的用来计算等效硫酸吗啡剂量;阿片类药物耐受的病人的程度;病人的一般情况和医疗状况;并发的药物;病人的疼痛的类型和严重性;风险因素滥用成瘾或转移,包括之前的滥用的历史中,成瘾或转移。以下推荐剂量,因此,只能被视为建议方法实际上是一个随着时间的推移的一系列临床决策的管理每个病人的痛苦。不断重新评估病人的接受tapentadol很重要,特别注意维护疼痛控制和副作用的相对发病率与治疗有关。在长期治疗,特别是对于non-cancer-related疼痛,定期评估持续使用阿片类止痛药的必要性。
期间改变镇痛需求,包括最初的滴定,频繁接触之间的推荐医生,医疗团队的其他成员,病人和照顾者/家庭。监测病人呼吸道或中枢神经系统抑郁的迹象。
2.2开始治疗
剂量为2.5毫升(相当于50毫克),3.75毫升(相当于75毫克),或5毫升(相当于100毫克)每4至6小时根据疼痛强度。
第一天的剂量,第二剂量可能管理第一剂量后一个小时,如果没有达到足够的疼痛与第一剂量。后续计量是2.5毫升(相当于50毫克),3.75毫升(相当于75毫克),或5毫升(相当于100毫克)每4至6小时,应该进行调整,以保持足够的镇痛与可接受的耐受性。
每日剂量大于700毫克第一天的治疗和600毫克在随后的日子还没有被研究过,不推荐。
NUCYNTA®可以有或没有食物(见临床药理学(12.3))。
2.3肾功能损害
使用NUCYNTA®有严重肾功能损害的患者不建议(见警告和注意事项(5.16)和临床药理学(12.3)]。
不推荐剂量调整患者的轻度或中度肾功能损害。
2.4肝损伤
的安全性和有效性NUCYNTA®还没有研究对严重肝损伤患者(儿童得分10 - 15)和使用在这个人口不推荐(见警告和注意事项(5.15))。
启动治疗对中度肝损伤患者与50毫克(儿童得分7 - 9)没有比每8小时更频繁(最多三个剂量在24小时内)。进一步治疗应该反映维护可接受的耐受性的镇痛是通过缩短或者延长给药间隔(见临床药理学(12.3))。
不推荐剂量调整患者的轻度肝损害(儿童得分5到6)(见临床药理学(12.3))。
2.5老年病人
一般来说,推荐剂量老年病人与正常肾和肝脏功能是一样的年轻成人患者与正常肾和肝脏功能。因为老年患者更有可能减少肾和肝脏功能,应该考虑从老年患者较低的推荐剂量范围。
2.6停止治疗
当病人与tapentadol不再需要治疗,逐渐减少剂量,防止戒断症状和体征病人身体上的依赖(见警告和注意事项(5.13))。
2.7说明使用
浓度和调剂:口服溶液包含20毫克每毫升tapentadol(毫升)和处方应写在毫升(毫升)和毫克(毫克)。口服注射器直接提供相应剂量是2.5毫升(= 50毫克)口服溶液,3.75毫升(等于75毫克)口服溶液,和5毫升口服溶液(等于100毫克)。
告知病人fda批准的病人标签的可用性,使用说明,一步一步的指示病人如何使用药瓶和口腔注射器。
-

维达Mia洗手液
![Vida Mia Hand Sanitizer (62%) (Alcohol) Gel [Navarro Discount Pharmacies,llc] 维达Mia洗手液(62%)(酒精)凝胶(纳瓦罗折扣药店,llc)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=b9057d3b-b104-4f09-8a61-c61ef9d4a3f3&name=canagliflozin-04.jpg)
2.1推荐剂量
的推荐起始剂量INVOKANA (canagliflozin)每日100毫克一次,在一天的第一顿饭。患者忍受INVOKANA 100毫克每天一次有60 mL / min / 1.73平方米的表皮生长因子受体或更高版本,需要额外的血糖控制,剂量可以增加到300毫克每天一次(见警告和注意事项(5.2),临床药理学(12.2),和病人咨询信息(17)]。
患者的体积损耗,纠正这种情况之前启动INVOKANA建议(见警告和注意事项(5.1),使用特定的人群(8.5和8.6),和病人咨询信息(17)]。
2.2患者肾功能损害
不需要剂量调整患者的轻度肾功能损害(60毫升/分钟/ 1.73平方米的表皮生长因子受体或更大)。
INVOKANA仅限于100毫克的剂量每天一次温和的肾功能损害患者的eGFR 45到不到60毫升/分钟/ 1.73平方米。
INVOKANA患者不应该发起一个eGFR不到45 mL / min / 1.73平方米。
评估肾功能建议INVOKANA治疗和定期启动之前。INVOKANA eGFR时应停止持续小于45 mL / min / 1.73平方米(见警告和注意事项(5.2)和使用在特定人群(8.6)]。
2.3同时使用UDP-Glucuronosyl转移酶(UGT)酶诱导物
如果ugt的诱导物(如利福平、苯妥英、镇静安眠剂,例如)与INVOKANA流行性流感减毒活疫苗,考虑增加病人目前的每日剂量300毫克一次容忍INVOKANA 100毫克每天一次有60 mL / min / 1.73平方米的表皮生长因子受体或更高,需要额外的血糖控制(见药物相互作用(7.1))。
考虑另一个患者的降糖药eGFR 45到不到60毫升/分钟/ 1.73平方米UGT诱导物,接受并发治疗。
-

毛霉
![Sporanox (Itraconazole) Solution [Janssen Pharmaceuticals, Inc.] 毛(伊曲康唑)解决方案(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=ae50721d-ee15-4ee7-9fe7-afd98c56461b&name=sporanox-02.jpg)
治疗口咽和食管念珠菌病
解决方案应该大力快速嘴里一次(10毫升)数秒,吞下。
推荐剂量的毛®(伊曲康唑)口腔口咽念珠菌病的解决方案是200毫克(20毫升)每天1到2周。口咽念珠菌病的临床症状和体征通常数天内解决。
口咽念珠菌病的患者反应迟钝/耐火材料与氟康唑片治疗,推荐剂量为100毫克(10毫升)b.i.d。患者对药物治疗的临床反应将在2 - 4周。患者中断治疗后不久就会复发。有限的数据对长期使用的安全性(> 6个月)的毛®口头解决方案是可用的。
推荐剂量的毛®口腔食道念珠菌病的解决方案是每天100毫克(10毫升)的最低治疗三周。应该继续治疗2周后解决的症状。剂量200毫克(每天20毫升)可以使用基于医学判断病人对治疗的反应。
毛®口服溶液和毛霉®胶囊不应交替使用。应指导患者采取毛®口服溶液没有食物,如果可能的话。只有毛®口头解决方案已经证明有效的口腔和食管念珠菌病。
肾功能损害患者使用
有限的数据可以使用口服伊曲康唑的患者肾功能损害。这种药物时应该小心谨慎管理患者人群。(见临床药理学:特殊人群和预防措施)。
在肝损伤患者使用
有限的数据可以使用口服伊曲康唑的患者的肝损伤。这种药物时应该小心谨慎管理患者人群。(见临床药理学:特殊人群、警告和预防措施)。
-

毛霉
![Sporanox (Itraconazole) Capsule [Janssen Pharmaceuticals, Inc.] 毛(伊曲康唑)胶囊(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=a4d555fa-787c-40fb-bb7d-b0d4f7318fd0&name=sporanox-02.jpg)
毛®(伊曲康唑)胶囊应采取一顿饱饭,至少可以保证最大吸收。毛®(伊曲康唑)必须吞下整个胶囊。
毛®胶囊是一个不同的准备比毛®口服溶液和不应交替使用。
芽生菌病的治疗和组织胞浆菌病
推荐剂量为200毫克每天一次(2胶囊)。如果没有明显的改善,或有证据表明进步的真菌疾病,100毫克的剂量应该增加增量最大的每天400毫克。剂量200毫克/天以上应在两个分裂的剂量。
曲霉病的治疗
每日推荐剂量的200到400毫克。
在危及生命的情况下治疗
在危及生命的情况下,应该使用负荷剂量。
虽然临床研究没有提供负荷剂量,建议,基于药代动力学数据,负荷剂量200毫克胶囊(2)每天三次(600毫克/天)治疗的前3天。
治疗应持续至少三个月,直到临床参数和实验室测试表明,活跃的真菌感染消退。一个疗程不足可能导致复发的活跃的感染。
毛®胶囊和毛霉®口服溶液不应交替使用。只有口头解决方案已经证明有效的口腔和食管念珠菌病。
治疗甲真菌病
脚趾甲有或没有指甲的参与:推荐剂量为200毫克胶囊(2)每天一次连续12周。
治疗甲真菌病
只指甲:推荐的给药方案是2治疗脉冲,每200毫克(2胶囊)b.i.d组成。(400毫克/天)1周。脉冲由三周期间没有毛®。
使用患者的肾功能损害:
有限的数据可以使用口服伊曲康唑的患者肾功能损害。这种药物时应该小心谨慎管理患者人群。(见临床药理学:特殊人群和预防措施)。
在肝损伤患者使用
有限的数据可以使用口服伊曲康唑的患者的肝损伤。这种药物时应该小心谨慎管理患者人群。(见临床药理学:特殊人群、警告和预防措施)。
-

Claravis
![Claravis (Isotretinoin) Capsule [Barr Laboratories, Inc.] Claravis(异维甲酸)胶囊(巴尔实验室,Inc .)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=b9057d3b-b104-4f09-8a61-c61ef9d4a3f3&name=canagliflozin-04.jpg)
2.1推荐剂量
的推荐起始剂量INVOKANA (canagliflozin)每日100毫克一次,在一天的第一顿饭。患者忍受INVOKANA 100毫克每天一次有60 mL / min / 1.73平方米的表皮生长因子受体或更高版本,需要额外的血糖控制,剂量可以增加到300毫克每天一次(见警告和注意事项(5.2),临床药理学(12.2),和病人咨询信息(17)]。
患者的体积损耗,纠正这种情况之前启动INVOKANA建议(见警告和注意事项(5.1),使用特定的人群(8.5和8.6),和病人咨询信息(17)]。
2.2患者肾功能损害
不需要剂量调整患者的轻度肾功能损害(60毫升/分钟/ 1.73平方米的表皮生长因子受体或更大)。
INVOKANA仅限于100毫克的剂量每天一次温和的肾功能损害患者的eGFR 45到不到60毫升/分钟/ 1.73平方米。
INVOKANA患者不应该发起一个eGFR不到45 mL / min / 1.73平方米。
评估肾功能建议INVOKANA治疗和定期启动之前。INVOKANA eGFR时应停止持续小于45 mL / min / 1.73平方米(见警告和注意事项(5.2)和使用在特定人群(8.6)]。
2.3同时使用UDP-Glucuronosyl转移酶(UGT)酶诱导物
如果ugt的诱导物(如利福平、苯妥英、镇静安眠剂,例如)与INVOKANA流行性流感减毒活疫苗,考虑增加病人目前的每日剂量300毫克一次容忍INVOKANA 100毫克每天一次有60 mL / min / 1.73平方米的表皮生长因子受体或更高,需要额外的血糖控制(见药物相互作用(7.1))。
考虑另一个患者的降糖药eGFR 45到不到60毫升/分钟/ 1.73平方米UGT诱导物,接受并发治疗。
-

Levaquin
![Levaquin (Levofloxacin) Tablet, Film Coated Levaquin (Levofloxacin) Solution Levaquin (Levofloxacin) Injection, Solution [Janssen Pharmaceuticals, Inc.] Levaquin(左氧氟沙星)平板电脑,薄膜涂层Levaquin(左氧氟沙星)解决方案Levaquin(左氧氟沙星)注射,解决方案(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=a1f01e8e-97e9-11de-b91d-553856d89593&name=levaquin-04.jpg)
2.1肾功能正常的成人患者的剂量
常规剂量的LEVAQUIN®平板电脑或口头解决方案是250毫克,500毫克,每24小时或750毫克口服,表示由感染和表1所示。常规剂量的LEVAQUIN®注入250毫克或500毫克由缓慢注入超过60分钟每24小时或750毫克每24小时由缓慢注入超过90分钟,表示由感染和表1所示。
这些建议适用于患者肌酐清除率≥50毫升/分钟。患者的肌酐清除率< 50毫升/分钟,调整药物剂量的要求(见剂量和管理(2.3))。
表1:成人患者的剂量正常肾功能(肌酐清除率≥50 mL / min)类型的感染*给每24小时持续时间(天)__ *由于指定病原体(参见适应症和用法(1))。†序贯疗法(静脉口服)可能制定了医生的自由裁量权。‡由于methicillin-susceptible金黄色葡萄球菌,肺炎链球菌(包括多重耐药性菌株分离[MDRSP])、流感嗜血杆菌、嗜血杆菌56,肺炎克雷伯菌,莫拉克斯氏菌属复活,Chlamydophila肺炎,嗜肺性军团菌、肺炎支原体(见适应症和使用(1.2))。§由于肺炎链球菌(不含多重耐药性菌株分离[MDRSP])、流感嗜血杆菌、嗜血杆菌56,肺炎支原体或肺炎Chlamydophila(参见适应症和使用(1.3))。¶这个方案表示cUTI由于大肠杆菌,肺炎克雷伯菌、变形杆菌和美联社由于大肠杆菌,包括例并发菌血症。#这方案是cUTI表示由于粪肠球菌、肠球菌泄殖腔,大肠杆菌,肺炎克雷伯菌、变形杆菌、绿脓假单胞菌;由于大肠杆菌和美联社。Þ药品管理局疑似或确诊后应尽快接触雾化炭疽杆菌。这个指标是基于代理端点。左氧氟沙星等离子体浓度实现人类合理地预测临床效益(见临床研究(14.9))。 ß The safety of LEVAQUIN ® in adults for durations of therapy beyond 28 days or in pediatric patients for durations beyond 14 days has not been studied. An increased incidence of musculoskeletal adverse events compared to controls has been observed in pediatric patients [see Warnings and Precautions (5.10), Use in Specific Populations (8.4), and Clinical Studies (14.9)]. Prolonged LEVAQUIN ® therapy should only be used when the benefit outweighs the risk. à Drug administration should begin as soon as possible after suspected or confirmed exposure to Yersinia pestis. Higher doses of LEVAQUIN ® typically used for treatment of pneumonia can be used for treatment of plague, if clinically indicated. Nosocomial Pneumonia 750 mg 7–14 Community Acquired Pneumonia‡ 500 mg 7–14 Community Acquired Pneumonia§ 750 mg 5 Acute Bacterial Sinusitis 750 mg 5 500 mg 10–14 Acute Bacterial Exacerbation of Chronic Bronchitis 500 mg 7 Complicated Skin and Skin Structure Infections (SSSI) 750 mg 7–14 Uncomplicated SSSI 500 mg 7–10 Chronic Bacterial Prostatitis 500 mg 28 Complicated Urinary Tract Infection (cUTI) or Acute Pyelonephritis (AP)¶ 750 mg 5 Complicated Urinary Tract Infection (cUTI) or Acute Pyelonephritis (AP)# 250 mg 10 Uncomplicated Urinary Tract Infection 250 mg 3 Inhalational Anthrax (Post-Exposure), adult and pediatric patients > 50 kg Þ,ß 500 mg 60ß Pediatric patients < 50 kg and ≥ 6 months of ageÞ,ß see Table 2 below (2.2) 60ß Plague, adult and pediatric patients > 50 kg à 500 mg 10 to 14 Pediatric patients < 50 kg and ≥ 6 months of age see Table 2 below (2.2) 10 to 142.2在儿科患者剂量
儿科患者的剂量≥6个月大的描述如下表2所示。
表2:在儿科患者剂量≥6个月大的类型的感染每时间__ * *剂量频率。由于炭疽杆菌(见适应症和使用(1.13))和鼠疫杆菌(参见适应症和使用(1.14))。†序贯疗法(静脉口服)可能制定了医生的自由裁量权。‡药品管理局疑似或确诊后应尽快接触雾化炭疽杆菌。这个指标是基于代理端点。左氧氟沙星等离子体浓度实现人类合理地预测临床效益(见临床研究(14.9)]§的安全LEVAQUIN®在儿科患者治疗的持续时间超过14天没有被研究过。增加肌肉骨骼不良事件的发生率比控制在儿科患者观察到(见警告和注意事项(5.10),使用特定的人群(8.4),(14.9)和临床研究)。长期LEVAQUIN®治疗时应只用于受益大于风险。¶药品管理局疑似或确诊后应尽快接触鼠疫杆菌。吸入的炭疽(接触后)‡§儿科患者> 50公斤500毫克24小时60天§儿科患者< 50公斤和≥6个月大的8毫克/公斤(不超过250毫克剂量)12小时60天§瘟疫¶儿科患者> 50公斤500毫克24小时10到14天儿科患者< 50公斤和≥6个月大的时候8毫克/公斤(不超过250毫克剂量)12人力资源10到14天2.3剂量调整成人肾损伤
小心管理LEVAQUIN®的肾功能不全。适当仔细的临床观察和实验室研究应该执行之前和期间自消除左氧氟沙星治疗可能减少。
不需要调整为患者肌酐清除率≥50毫升/分钟。
患者受损的肾功能(肌酐清除率< 50毫升/分钟),调整给药方案是必要的,以避免左氧氟沙星的积累由于减少间隙(见使用在特定的人群(8.6))。
表3显示了如何调整剂量根据肌酐清除率。
表3:剂量调整成人患者的肾功能损害(肌酐清除率< 50 mL / min)剂量每24小时在正常肾功能肌酐Clearance20 49 mL / min肌酐Clearance10 19 mL / min血液透析或慢性腹膜透析(李)750毫克750毫克每48小时750毫克初始剂量,然后500毫克每48小时750毫克初始剂量,然后500毫克每48小时500毫克500毫克初始剂量,然后250毫克每24小时500毫克初始剂量,然后250毫克每48小时500毫克初始剂量,然后250毫克每48小时250毫克每48小时不需要调整剂量250毫克。如果治疗简单的泌尿道感染,那么不需要剂量调整剂量调整可用的任何信息2.4药物相互作用与螯合剂的药物:抗酸药、硫糖铝、金属阳离子、复合维生素
LEVAQUIN®平板电脑和口腔的解决方案
LEVAQUIN®平板电脑和口服溶液应至少前两小时或两小时后抗酸药含镁、铝、硫糖铝、金属阳离子如铁,锌和维生素制剂或必要/缓冲片或儿科粉口服溶液(见药物相互作用(7.1)(17.2)]和病人咨询信息。
LEVAQUIN®注入
LEVAQUIN®注入流行性流感减毒活疫苗不应与含有多价阳离子的任何解决方案,例如,通过相同的静脉镁、线(见剂量和管理(2.6))。
2.5管理指令
食品和LEVAQUIN®平板电脑和口腔的解决方案
LEVAQUIN®平板电脑可以不考虑食品管理。建议LEVAQUIN®口服溶液被前1小时或2小时后进食。
LEVAQUIN®注入
警告:快速或丸静脉注入LEVAQUIN®与低血压有关,必须避免。LEVAQUIN®注射应该慢慢注入静脉注射在一段不少于60或90分钟,这取决于剂量。LEVAQUIN®注射应只能由静脉输液。它不是为肌内,鞘内、腹腔内或皮下管理。
水化对病人接受LEVAQUIN®平板电脑,口服溶液,注入
接受口服或静脉注射的患者充分水化LEVAQUIN®应该维护,以防止高度浓缩尿液的形成。结晶尿管型尿报告和喹诺酮类(见不良反应(6.1)(17.2)]和病人咨询信息。
2.6制备静脉注射产品
注射用药物的药物产品应检查视觉颗粒物和变色政府之前,每当解决方案和容器许可证。
因为只有有限的数据可用的兼容性LEVAQUIN®和其他静脉注射物质、添加剂或其他药物不应该被添加到LEVAQUIN®注入预混料在一次性灵活的容器,或通过相同的同时注入静脉注射线。如果相同的静脉注射线是用于连续注入的几种不同的药物,这条线应该刷新之前和之后注入LEVAQUIN®注射和输液兼容LEVAQUIN®注入和与其他药物(s)管理通过这种常见的线。
LEVAQUIN®注入预混料在一次性灵活的容器(5毫克/毫升)
LEVAQUIN®注入中提供灵活的容器内衬托外包装。这些包含预先混合,可以使用左氧氟沙星在5%葡萄糖(D5W)一次性的解决方案。100毫升预拌柔性容器包含250毫克/ 50毫升或500毫克/ 100毫升的左氧氟沙星的解决方案。150毫升柔性容器包含750毫克/ 150毫升的左氧氟沙星的解决方案。每个容器的浓度为5毫克/毫升。没有进一步稀释这些准备工作是必要的。因为预混料柔性容器仅供一次性使用,任何未使用的部分应该被丢弃。
指令使用LEVAQUIN®注入预混料在灵活的容器:
撕裂外切口和删除解决方案容器包装。检查容器的分钟泄漏坚定地通过挤压内袋。如果发现泄漏,或者密封不完整,丢弃的解决方案,为不育可能就会大打折扣。不要使用如果解决方案是多云或沉淀。使用无菌设备。警告:不要使用灵活的容器串联连接。这样的使用可能导致空气栓塞由于残余空气从主容器之前政府的液体从二级容器就完成了。准备管理:
关闭流控制管理夹集。将覆盖从港口在容器的底部。穿刺销管理组插入端口与扭转运动,直到销坚定地坐着。注意:看到完整的管理方向集箱。暂停从衣架容器。紧缩和释放排水室建立合适的液面在输液室的LEVAQUIN®注入预混料在灵活的容器。打开流控制夹从组排出空气。关闭夹。规范的管理与流量控制夹。 -

Terazol 7
![Terazol 7 (Terconazole) Cream Terazol 3 (Terconazole) Cream Terazol 3 (Terconazole) Suppository [Janssen Pharmaceuticals, Inc.] Terazol 7 (Terconazole)奶油Terazol 3 (Terconazole)奶油Terazol 3 (Terconazole)栓剂(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=6f2626b3-6053-4f7a-bc5d-78e30d983f90&name=terazol-10.jpg)
TERAZOL®7 (terconazole)阴道奶油0.4%
一个完整器(5克)TERAZOL®7阴道乳膏(20毫克terconazole)应阴道内的连续七天每天睡前一次。
TERAZOL®3 (terconazole)阴道奶油0.8%
一个完整器(5克)TERAZOL®3阴道乳膏(40毫克terconazole)应阴道内的睡前每天一次连续三天。
TERAZOL®3 (terconazole)阴道栓剂80毫克
一个TERAZOL®3阴道栓剂(80毫克terconazole)应该管理阴道内的睡前每天一次连续三天。
处方治疗的另一个课程之前,应该再次得到涂片诊断和/或文化和其他病原体通常与外阴阴道炎有关排除。这些产品的治疗效果不受月经的影响。
-

片剂
![Ultram (Tramadol Hydrochloride) Tablet, Coated [Janssen Pharmaceuticals, Inc.] 片剂(盐酸曲马多)平板涂布(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=45f59e6f-1794-40a4-8f8b-3a9415924468&name=ultram-04.jpg)
(17岁及以上的成人)
适度中度到严重的慢性疼痛患者不需要快速的镇痛效果,片剂的耐受性®可以提高初始治疗以下滴定方案:片剂®应该开始在25毫克/天qAM和滴定25 mg增量作为单独的剂量每3天达到100毫克/天(25毫克q.i.d)。此后每日总剂量可以增加50毫克容忍每3天达到200毫克/天(50毫克q.i.d)。滴定后,片剂®50至100毫克可以作为缓解疼痛所需管理每4至6小时不超过400毫克/天。
子集的病人来说,快速出现镇痛效果是必需的和为谁的利益大于风险停止由于与更高的初始剂量相关的不良事件,片剂®50毫克至100毫克可以作为缓解疼痛所需管理每四到六个小时,每天不超过400毫克。
个性化的剂量
良好的疼痛管理实践规定剂量根据患者需要使用个性化的最低剂量有益。与曲马多在成人的研究表明从最低的剂量和滴定上升将导致更少的中止和耐受性的增加。
在所有患者肌酐清除率不到30毫升/分钟,建议的剂量间隔片剂®是增加到12个小时,最大程度上的每日剂量为200毫克。因为只有7%的服用剂量是被血液透析,透析病人可以接受常规剂量在透析。成人肝硬化患者推荐剂量为50毫克每12小时。一般来说,剂量选择一位上了年纪的病人超过65岁应该谨慎,通常开始在低端的剂量范围,反映了更大的频率减少肝脏、肾脏或心脏功能和伴随疾病或其他药物治疗。对老年病人超过75岁,总剂量不应超过300毫克/天。 -

片剂呃
![Ultram Er (Tramadol Hydrochloride) Tablet, Extended Release [Janssen Pharmaceuticals, Inc.] 片剂Er(盐酸曲马多)平板电脑,延长释放(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=039f9e7c-97f5-4062-8656-6f355c82008e&name=ultram-er-06.jpg)
片剂ER在患者不应使用:
•肌酐清除率不到30 mL / min,•严重肝损伤(儿童类C)(参见预防措施,使用在肾和肝脏疾病)。
片剂ER必须吞下整个不能咀嚼,压碎,或者分裂(看到警告,误用,滥用和阿片类药物和药物滥用和成瘾的转移)。
成年人(18岁以上)
患者对曲马多速产品目前没有
患者目前还没有治疗曲马多速(IR)产品,片剂ER应发起每日剂量为100毫克一次,滴定所必要的100毫克每五天的增量来缓解疼痛和根据耐受性。片剂ER不应服用剂量超过300毫克每天。
患者目前曲马多速产品
对曲马多的患者保持红外产品,计算24小时剂量曲马多红外和启动每日总剂量的片剂ER四舍五入到下一个最低100毫克增量。剂量可能随后根据病人个性化的需要。由于局限性与片剂剂量选择的灵活性,一些病人保持对曲马多红外产品可能无法转换为片剂。片剂ER不应服用剂量超过300毫克每天。片剂的伴随使用ER与其他曲马多产品不推荐(见警告)。
个性化的剂量
良好的疼痛管理实践规定剂量根据患者需要使用个性化的最低剂量有益。最低的剂量滴定向上而容忍达到一个适当的效果。临床研究的片剂ER没有表现出临床受益每日总剂量超过300毫克。
一般来说,一位上了年纪的病人的剂量(超过65岁)应该开始谨慎,通常开始在低端的剂量范围,反映了更大的频率降低肝脏、肾脏或心脏功能和伴随疾病或其他药物治疗。片剂ER应与75多年的患者中更加谨慎,由于更大的不良事件出现的频率在这个人口。
-

Axert
![Axert (Almotriptan Malate) Tablet, Coated [Janssen Pharmaceuticals, Inc.] Axert (Almotriptan酸盐)平板涂布(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=a8479ec0-204e-11e1-aa3f-a3c74724019b&name=axert-05.jpg)
2.1急性治疗偏头痛的原因
的推荐剂量AXERT®(almotriptan酸盐)在成人和12到17岁的青少年是6.25毫克到12.5毫克,12.5毫克剂量往往会更有效剂量的成年人。作为个体的应对不同剂量可能不同AXERT®,剂量的选择应该基于一个人的。
如果头痛缓解在最初AXERT®剂量但回报,2小时后的剂量可能重复。第二个剂量的有效性尚未建立于安慰剂对照试验。最大程度上的每日剂量不应超过25毫克。安全的治疗平均超过4偏头痛在30天内还未确定。
2.2肝损伤
的推荐起始剂量AXERT®肝损伤患者是6.25毫克。最大程度上的每日剂量不应超过12.5毫克的24小时(见警告和注意事项(5.9)和临床药理学(12.3)]。
2.3肾功能损害
的推荐起始剂量AXERT®有严重肾功能损害的患者是6.25毫克。最大程度上的每日剂量不应超过12.5毫克的24小时(见警告和注意事项(5.9)和临床药理学(12.3)]。
-

Duragesic
![Duragesic (Fentanyl) Patch [Janssen Pharmaceuticals, Inc.] Duragesic(芬太尼)补丁(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=d7aade83-9e69-4cd5-8dab-dbf1d7b89bb4&name=duragesic-14.jpg)
2.1初始计量
DURAGESIC规定只有通过医疗保健专业人士应该知识渊博的使用强效阿片类药物对慢性疼痛的管理。
由于呼吸抑郁的风险,DURAGESIC只是用于病人已经opioid-tolerant表示。停止或锥形其他延长释放阿片类药物时开始DURAGESIC疗法。DURAGESIC只有用于opioid-tolerant病人,不要开始任何病人DURAGESIC第一阿片样物质。
病人认为opioid-tolerant是那些正在每天至少60毫克的吗啡,或者至少30毫克口服羟考酮日报,每天或至少8毫克口服hydromorphone或equianalgesic剂量的阿片类药物一周或更长时间。
单独启动每个患者的给药方案,考虑到病人的镇痛治疗经验和成瘾的风险因素,滥用和误用(见警告和注意事项(5.1))。密切监测患者呼吸道抑郁症,特别是24 - 72小时内开始治疗时DURAGESIC血清浓度从最初的补丁峰值(见警告和注意事项(5.2))。
转换时的推荐起始剂量与其他阿片类药物DURAGESIC旨在最小化潜在的第一个患者用药剂量。
DURAGESIC时停止所有其他阿片药物治疗开始。
虽然有有用的阿片等价物现成的表,有大量inter-patient可变性的相对效力不同的阿片类药物和产品。因此,它比低估患者24小时芬太尼要求并提供救援药物(如速阿片)比高估了24小时芬太尼需求导致不良反应。DURAGESIC临床试验中,患者从他们之前阿片DURAGESIC使用转换表1的指导初始DURAGESIC剂量。beplay体验
表1中使用的信息时考虑以下:
这不是一个表equianalgesic剂量。转换剂在这个表只是转换从一个上市的口服或肠外DURAGESIC阿片类止痛药。表从DURAGESIC不能用于转换到另一个阿片样物质。这样做会导致过高的剂量的阿片类药物,并可能导致致命的过量。将病人从口服或肠外DURAGESIC阿片类药物,用表1。不要用表1从DURAGESIC转换到其他疗法,因为这种转换DURAGESIC保守,会高估新代理的剂量。
表1 *:每日剂量转换DURAGESIC当前镇痛剂量(毫克/天)另外,成人和儿科病人服用阿片类药物或剂量表1中没有列出,使用上述转换方法和表2。表1 *不应该用来从DURAGESIC转换到其他疗法因为DURAGESIC这种转换是保守的。使用的表1转换为其他镇痛疗法可以高估新代理的剂量。过剂量的止痛剂是可能的(见剂量和管理(2.3))。口服吗啡60 - 134 135 - 224 225 - 314 315 - 404肌内或静脉注射吗啡10-22 23-37 38-52 53 - 67口服羟考酮30 - 67 67.5 -112 112.5 -157 157.5 -202年口腔可待因口服hydromorphone 150 - 447 8 - -51 17.1 -28 28.1 -39 39.1静脉hydromorphone 1.5 -3.4 3.5 -5.6 5.7 -7.9 8 - 10肌内哌替啶75 - 165 166 - 278 279 - 390 391 - 503口服美沙酮20-44 45 - 74 75 - 104 105 - 134⇓⇓⇓⇓DURAGESIC推荐剂量25微克/小时50毫克/ 75微克/小时100微克/小时另外,对于成人和儿科病人服用阿片类药物或剂量表1中没有列出,使用以下方法:
1。计算前24小时镇痛的要求。2。这个量转换为equianalgesic口服吗啡剂量使用一个可靠的参考。请参考表2的24小时口服吗啡剂量范围,建议每个DURAGESIC剂量转换。用这个表来找到24小时的吗啡剂量和相应的DURAGESIC剂量计算。发起DURAGESIC治疗使用推荐剂量和滴定向上病人频繁(不超过3天在最初的剂量和每6天之后)直到达到止痛功效。
3所示。表2不使用从DURAGESIC转换到其他疗法因为DURAGESIC这种转换是保守,会高估新代理的剂量。表2 *:推荐初始DURAGESIC剂量根据每日口服吗啡剂量口服24-hourMorphine(毫克/天)DURAGESICDose(微克/小时)注:在临床试验中,这些范围的每日口服吗啡剂量使用DURAGESIC作为转换的基础。表2 *不应该用来从DURAGESIC转换到其他疗法因为DURAGESIC这种转换是保守的。使用表2转换到其他镇痛疗法可以高估新代理的剂量。过剂量的止痛剂是可能的(见剂量和管理(2.5))。60 - 134 25 135 - 224 50 225 - 314 75 315 - 404 100 405 - 494 125 495 - 584 150 585 - 674 175 675 - 764 200 765 - 854 225 855 - 944 250 945 - 1034 275 1035 - 1124 300交付率超过100微克/小时,可以使用多个系统。
肝损伤
避免使用DURAGESIC患者严重的肝损伤。轻度至中度肝损害患者,开始与一个DURAGESIC常规剂量的一半。密切监控镇静和呼吸抑郁症的迹象,包括在每个剂量增加(见警告和注意事项(5.14),使用特定的人群(8.6)和临床药理学(12.3)]。
肾功能损害
避免使用DURAGESIC有严重肾功能损害的患者。轻度至中度患者的肾功能损害,开始与一个DURAGESIC常规剂量的一半。密切监控镇静和呼吸抑郁症的迹象,包括在每个剂量增加(见警告和注意事项(5.15),使用特定的人群(8.7)和临床药理学(12.3)]。
2.2滴定和维护治疗
分别滴定DURAGESIC提供足够的镇痛的剂量和最大限度地减少不良反应。不断地重新评估患者接受DURAGESIC评估疼痛控制的维护和相关不良反应的发生率,以及监测成瘾的发展,滥用或误用。频繁的开药者之间的沟通是很重要的,医疗保健团队的其他成员,病人和照顾者/家庭期间改变镇痛需求,包括最初的滴定。在长期治疗,定期评估持续阿片类止痛药的必要性。
DURAGESIC剂量间隔是72小时。不增加DURAGESIC首次剂量,直到至少3天在最初的应用程序。滴定剂量每日剂量的基础上补充患者所需的阿片类止痛药的第二或第三天的初始应用程序。
它可能需要6天对新剂量芬太尼水平达到平衡(见临床药理学(12.3))。因此,评估患者进一步滴定后不少于两个为期3天的应用程序之前任何进一步增加剂量。
基地剂量增加补充每日剂量的阿片类药物,使用的比例45毫克/ 24小时口服吗啡DURAGESIC 12 mcg /小时增加剂量。
如果不能接受opioid-related不良反应观察,随后的剂量可能会减少。调整剂量以获得一个适当的平衡管理的痛苦和opioid-related不良反应。
一小部分的成年患者可能不使用72小时达到充分镇痛剂量间隔和可能需要系统应用在48个小时而非72个小时,只有足够的疼痛控制无法实现使用一个72小时的疗程。DURAGESIC剂量的增加应该改变之前评估剂量间隔为了维持病人72小时的方案。
给药间隔少于每72小时没有研究在儿童和青少年,不推荐。
2.3管理DURAGESIC
DURAGESIC补丁仅供皮肤使用。
妥善处理DURAGESIC是必要的,以防止严重不良的结果,包括死亡,意外二级接触DURAGESIC(见警告和注意事项(5.3))。
应用程序和处理指令
病人应该应用DURAGESIC完好无损,non-irritated non-irradiated皮肤放在一个平面上,如胸部,背部,侧面或上臂。在幼儿和认知障碍的人,附着力应监测和上背部是首选的位置以减少潜在的不恰当的补丁。在应用程序网站可能会剪头发之前(不刮)系统应用程序。如果DURAGESIC的网站应用程序必须被净化的应用补丁之前,用清水。不要使用肥皂、油、乳液、酒精、或任何其他的代理可能会刺激皮肤或改变它的特性。让皮肤完全干燥之前补丁程序。病人应该适用DURAGESIC密封包装后立即删除。补丁一定不能改变(例如,削减)以任何方式之前,应用程序。DURAGESIC不应使用如果袋密封坏了或者补丁是削减或损坏。皮肤系统按的手坚定地用手掌在30秒,确保完成接触,尤其是边缘。 Each DURAGESIC patch may be worn continuously for 72 hours. The next patch is applied to a different skin site after removal of the previous transdermal system. If problems with adhesion of the DURAGESIC patch occur, the edges of the patch may be taped with first aid tape. If problems with adhesion persist, the patch may be overlayed with a transparent adhesive film dressing. If the patch falls off before 72 hours, dispose of it by folding in half and flushing down the toilet. A new patch may be applied to a different skin site. Patients (or caregivers who apply DURAGESIC) should wash their hands immediately with soap and water after applying DURAGESIC. Contact with unwashed or unclothed application sites can result in secondary exposure to DURAGESIC and should be avoided. Examples of accidental exposure include transfer of a DURAGESIC patch from an adult's body to a child while hugging, sharing the same bed as the patient, accidental sitting on a patch and possible accidental exposure of a caregiver's skin to the medication in the patch while applying or removing the patch. Instruct patients, family members, and caregivers to keep patches in a secure location out of the reach of children and of others for whom DURAGESIC was not prescribed.避免热
指导患者避免暴露DURAGESIC应用站点及周边区域的直接外部热源,如电热垫或电热毯,热或晒黑灯,日光浴,热水澡,桑拿浴室,热水浴缸,和加热水床,穿着系统(见警告和预防措施(5。11)]。
2.4处理指令
未能妥善处置DURAGESIC导致意外曝光和死亡(见警告和注意事项(5.3))。
病人应该处理补丁后立即删除使用折叠贴片胶的一面,然后冲洗厕所。
未使用的补丁应该从他们的袋,保护衬垫,补丁折叠,粘合的补丁坚持本身,并立即冲进厕所。
病人应该处理任何补丁剩余的处方就不再需要。
2.5中止DURAGESIC
大量的从皮肤吸收芬太尼继续删除补丁后24小时或更多(见临床药理学(12.3))。
将病人到另一个阿片样物质,去除DURAGESIC和滴定剂量的镇痛基于病人的报告的疼痛,直到足够的镇痛。在系统删除,17个小时或更多需要降低50%血清浓度芬太尼。戒断症状可能在一些病人剂量转换或调整(见警告和注意事项(5.17))。
不要用表1和2从DURAGESIC转换到其他疗法避免高估新代理的剂量可能导致过量的镇痛和死亡。
当中断DURAGESIC而不是转换到另一个阿片类药物,使用逐步向下的滴定,例如减半剂量每6天,为了减少戒断症状的可能性(见警告和注意事项(5.17))。尚不清楚在什么剂量水平DURAGESIC可能没有停止生产阿片戒断症状和体征。
-
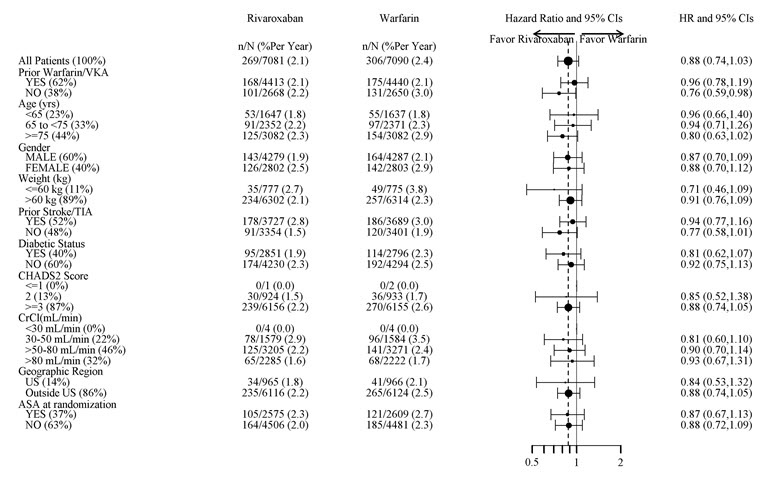
Xarelto
![Xarelto (Rivaroxaban) Tablet, Film Coated Xarelto (Rivaroxaban) Kit [Janssen Pharmaceuticals, Inc.] Xarelto (Rivaroxaban)平板电脑,薄膜涂层Xarelto (Rivaroxaban)工具包(詹森制药有限公司)](http://dailymed.nlm.nih.gov/dailymed/image.cfm?setid=10db92f9-2300-4a80-836b-673e1ae91610&name=xarelto-06.jpg)
表明在非瓣膜性房颤剂量减少中风的风险(2.3)CrCl > 50毫升/分钟:20毫克每天一次的晚餐CrCl 15到50毫升/分钟:15毫克每天一次的晚餐治疗深静脉血栓形成(2.4)治疗PE(2.4) 15毫克每日两次食物,第一21天▼21天后,过渡到▼20毫克每天一次食物,其余治疗深静脉血栓形成和复发的风险减少PE(2.4) 20毫克每天一次食物后深静脉血栓形成的预防髋关节或膝关节置换手术(2.5)髋关节置换:10毫克每天一次35天膝盖替换:10毫克每日一次,12天
2.1重要的食品影响的信息
15毫克,20毫克XARELTO平板电脑应该用食物,而10毫克的平板电脑可以有或没有食物(见临床药理学(12.3))。
非瓣膜性房颤的疗效研究XARELTO用晚餐。
2.2与XARELTO切换
从华法林转向XARELTO——切换时患者华法林XARELTO,尽快停止华法林,开始XARELTO国际标准化比率(INR)低于3.0,以避免时间的抗凝不足。
从XARELTO转向华法林——没有临床试验数据可用于指导将病人从XARELTO华法林。beplay体验XARELTO影响INR,所以INR测量在共同服用华法林不得用于确定适当的华法林剂量。一种方法是停止XARELTO并开始注射用药物的抗凝和华法林当时的下一剂量XARELTO拍摄。
从XARELTO转向除了华法林抗凝血剂,患者目前XARELTO和过渡到一种抗凝快速开始,停止XARELTO和其他给第一剂量的抗凝剂(口服或肠外),下一个XARELTO剂量会被(见药物相互作用(7.3))。
从除了华法林抗凝血剂转向XARELTO——患者接受非华法林的抗凝剂,目前,开始XARELTO 0到2小时前下安排晚上管理药物(例如,低分子量肝素或non-warfarin口服抗凝剂)和省略其他抗凝管理。依诺肝素是由连续注入,停止输液并开始XARELTO在同一时间。
非瓣膜性房颤2.3
患者的肌酐清除率(CrCl) > 50毫升/分钟,XARELTO的推荐剂量20毫克每日口服一次晚餐。患者CrCl 15到50毫升/分钟,推荐的剂量是15毫克每天一次的晚餐(见使用在特定的人群(8.7))。
2.4治疗深静脉血栓形成(DVT),减少肺栓塞(PE), PE的深静脉血栓形成和复发的风险
推荐剂量的XARELTO初始治疗急性深静脉血栓形成和/或PE 15毫克口服每日两次食物第一21天。这个最初的治疗期后,推荐剂量的XARELTO 20毫克口服一次日常食物,每天大约在同一时间。XARELTO的推荐剂量减少再次发生深静脉血栓形成的风险或PE 20毫克口服一次日常食物每天大约在同一时间(见临床研究(14.2))。
2.5预防深静脉血栓形成后髋关节或膝关节置换手术
的推荐剂量XARELTO 10毫克口服一次每日有或没有食物。初始剂量应采取6至10个小时手术后,建立了止血(见剂量和管理(2.6))。
对于接受髋关节置换手术的患者,建议治疗持续时间35天。对于接受膝关节置换手术的患者,建议治疗持续时间12天。2.6中止手术和其他干预措施
如果必须停止抗凝治疗来减少出血的风险与手术或其他程序,XARELTO应该停止前至少24小时的过程减少出血的风险(见警告和注意事项(5.2))。在决定一个过程是否应该推迟到24小时XARELTO最后剂量后,需权衡出血的风险增加的紧迫性干预。XARELTO手术后应重新启动或其他程序已经建立了足够的止血,注意时间的治疗效果是短暂的(见警告和注意事项(5.1))。如果无法在口服药物或手术治疗后,考虑管理肠外抗凝。
2.7错过剂量
如果一个剂量的XARELTO没有在预定的时间,尽快管理剂量在同一天如下:
病人接受15毫克每日两次:病人应该立即XARELTO确保摄入30毫克每天XARELTO。在这个特定的实例,两个15毫克平板电脑可以。病人应该继续定期15毫克每日推荐摄入量为第二天的两倍。病人接受20毫克,15毫克或10毫克每天一次:病人应该立即错过XARELTO剂量。2.8管理选项
的患者无法吞下整个平板电脑,10毫克,15毫克或20毫克XARELTO平板电脑可能会粉碎和混合使用前迅速苹果酱和口服药物。政府后碎XARELTO 15毫克或20毫克的平板电脑,剂量应立即紧随其后的是食物(见剂量和管理(2.1,2.3,2.4)和临床药理学(12.3)]。
政府通过鼻胃管(NG)或胃饲管:证实胃管的位置后,10毫克,15毫克或20毫克XARELTO平板电脑可能会碎,悬浮在50毫升的水和管理通过一个NG管或胃饲管。自rivaroxaban吸收取决于药物的释放,避免管理XARELTO远端胃可以导致减少吸收,从而,减少药物暴露。政府后碎XARELTO 15毫克或20毫克的平板电脑,剂量应该立即紧随其后的是肠内喂养(见临床药理学(12.3))。
碎10毫克,15毫克或20毫克XARELTO平板电脑是稳定在水和苹果酱长达4个小时。一项体外相容性研究表明没有吸附的rivaroxaban水碎XARELTO平板的悬浮PVC或硅胶鼻胃管(NG)。
注册一个免费帐户







