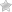FDA记录显示没有目前的这种药物回忆说。beplay sport中心钱包
你是医学专业吗?
盐酸表柔比星回忆
得到一个警告当一个回忆。
问题&答案
副作用和不良反应
盐酸表柔比星注射液应只有合格的医生的监督下使用细胞毒性治疗经验。在开始用盐酸表柔比星治疗之前,患者应该恢复急性毒性(如性口炎、中性粒细胞减少、血小板减少和广义感染)之前的细胞毒性治疗。同时,初始注射用盐酸表柔比星治疗之前应仔细基线评估血液计数;血清总胆红素水平、AST和肌酐;和心脏功能以左心室射血功能(LVEF)。应该小心地监视病人治疗期间可能由于myelosuppression临床并发症。支持性护理可能是必要的治疗严重中性粒细胞减少和严重的感染性并发症。监测潜在的毒性也很重要,尤其是在更大的累积暴露于盐酸表柔比星。
存在剂量依赖的相关性,可逆的白血球减少症和/或嗜中性白血球减少症的主要表现是血液毒性与表柔比星,代表了最常见的急性dose-limiting这种药物的毒性。在大多数情况下,白细胞(WBC)达到最低点从药品管理局10到14天。白血球减少症/嗜中性白血球减少症通常是短暂的,白细胞和中性粒细胞计数一般恢复正常价值由药品监督管理局后21天。与其他细胞毒性剂,盐酸表柔比星注射液结合推荐剂量的环磷酰胺和氟尿嘧啶可以产生严重的白血球减少症和嗜中性白血球减少症。还可能出现严重的血小板减少症和贫血。临床后果严重的myelosuppression包括发烧、感染、败血症、感染性休克、出血,组织缺氧,贫血症状,甚至死亡。如果myelosuppressive并发症发生,适当的支持措施(例如,静脉注射抗生素、集落刺激因子、输血)可能是必需的。Myelosuppression需要仔细监测。道达尔和微分的白细胞,红细胞(RBC)和血小板计数应该评估之前和期间每个周期与盐酸表柔比星注射液治疗。
毒性是一个已知的蒽环霉素治疗的风险。Anthracycline-induced心脏毒性可以通过早期(或急性)或晚期(延迟)事件。盐酸表柔比星的早期心脏毒性主要由窦性心动过速和/或心电图异常等非特异性ST-T波变化,但快速性心律失常,包括过早心室收缩和室性心动过速、心动过缓、以及房室束支块也被报道。这些影响通常不延迟毒性预测后续发展,临床重要性的很少,一般不考虑暂停的指示表柔比星治疗。延迟心脏毒性结果特征所体现的心肌病LVEF减少和/或充血性心力衰竭(CHF)的症状和体征如心动过速、呼吸困难、肺水肿,依赖水肿、肝肿大、腹水,胸腔积液,奔马律。危及生命的瑞士法郎是anthracycline-induced心肌病最严重的形式。这种毒性似乎依赖于累积剂量盐酸表柔比星注射液和代表药物的累积dose-limiting毒性。如果它发生,延迟毒性通常发展后期与盐酸表柔比星注射液在治疗的过程中或完成后2到3个月内治疗,但后来事件(几个月年治疗后终止)的报告。
回顾性调查,包括9144个病人,大多在晚期实体肿瘤,发展瑞士法郎的概率增加而增加累积剂量盐酸表柔比星注射液(图5)。epirubicin-treated患者的估计风险发展临床明显的瑞士法郎是0.9%的累积剂量550毫克/米2,1.6%在700毫克/米2,3.3%在900毫克/米2。患心力衰竭的风险在缺乏其他心脏风险因素急剧增加后表柔比星的累积剂量900毫克/米2。
在另一个469年回顾性调查epirubicin-treated转移或早期乳腺癌患者,瑞士法郎的报道风险相媲美,在更大的超过9000名患者的研究。
鉴于心肌病的风险,累积剂量为900毫克/米2盐酸表柔比星注射液应超过只有极其谨慎。心血管疾病危险因素(积极或休眠,之前或伴随纵隔放疗/心包,先前的疗法与其他蒽环霉素或anthracenediones,同时使用其他药物能够抑制心脏收缩性)可能会增加心脏毒性的风险。虽然没有正式测试,很可能,表阿霉素的毒性和其他蒽环霉素或anthracenediones添加剂。心脏毒性与盐酸表柔比星注射液可能发生在较低累积剂量是否心脏危险因素存在。
尽管endomyocardial活检被认为是最敏感的诊断工具来检测anthracycline-induced心肌病,实际上这种侵入性检查并不表现在日常的基础上。心电图(ECG)改变如心律失常、QRS电压的降低,或延长超出正常范围的收缩时间间隔anthracycline-induced心肌病可能暗示,但心电图不是一个敏感的或特定的方法后anthracycline-related毒性。严重心脏损害的风险可以通过定期监测LVEF减少治疗过程中及时停药盐酸表柔比星注射液在第一个功能受损的迹象。重复评估心脏功能的首选方法是评价LVEF衡量multi-gated放射性核素血管造影术(蒙加)或超声心动图(回声)。基线评估心脏的心电图和蒙加扫描或建议一个回声,尤其是在患者的危险因素增加心脏毒性。重复蒙加或回声LVEF应该执行的决定,特别是在高,累积蒽环霉素剂量。该技术用于评估通过后续应该是一致的。患者的危险因素,尤其是蒽环霉素或anthracenedione使用之前,心脏功能必须是特别严格的监测和风险-效益持续注射用盐酸表柔比星治疗的患者心脏功能受损必须仔细评估。
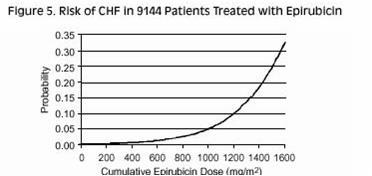
二次急性骨髓性白血病的发生,有或没有一个preleukemic阶段,患者被报道在蒽环霉素。继发性白血病时更常见的这类药物结合能损伤dna的抗肿瘤的药物,当病人已经大量使用细胞毒性药物,或者当剂量的蒽环霉素已经升级。这些白血病可以有短1 - 3年的潜伏期。分析7110例接受辅助治疗与表柔比星在控制临床试验的一个组成部分poly-chemotherapy方案对于早期乳腺癌,显示累计二次急性骨髓性白血病或骨髓增生异常综合征的风险(AML / MDS)约0.27%的(大概95%可信区间,0.14至0.40)3年,0.46%(大概95%可信区间,0.28至0.65),5年和0.55%(大概95%可信区间,0.33至0.78)8年。的风险开发AML / MDS盐酸表柔比星累积剂量的增加而增加,如图6所示。
发展AML / MDS的累积概率被发现在病人特别增加超过表柔比星的最大推荐累积剂量(720毫克/米2)或环磷酰胺(6300毫克/米2),如表4所示。
| 年从治疗开始 | 累积概率的AML / MDS %(95%置信区间) | |||
|---|---|---|---|---|
| 环磷酰胺累积剂量≤6300毫克/米2 | 环磷酰胺累积剂量> 6300毫克/米2 | |||
| 盐酸表柔比星累积剂量 | 盐酸表柔比星累积剂量 | 盐酸表柔比星累积剂量 | 盐酸表柔比星累积剂量 | |
| ≤720毫克/米2 | > 720毫克/米2 | ≤720毫克/米2 | > 720毫克/米2 | |
| N = 4760 | N = 111 | N = 890 | N = 261 | |
| 3 | 0.12 (0.01 - 0.22) | 0.00 (0.00 - 0.00) | 0.12 (0.00 - 0.37) | 4.37 (1.69 - 7.05) |
| 5 | 0.25 (0.08 - 0.42) | 2.38 (0.00 - 6.99) | 0.31 (0.00 - 0.75) | 4.97 (2.06 - 7.87) |
| 8 | 0.37 (0.13 - 0.61) | 2.38 (0.00 - 6.99) | 0.31 (0.00 - 0.75) | 4.97 (2.06 - 7.87) |
盐酸表柔比星注入诱变、致染色体断裂的和动物致癌(见下一节,致癌作用,诱变和生育障碍)。
治疗相关的急性骨髓性白血病一直在报道女性对待epirubicin-based辅助化疗方案(见上节中,警告,二次白血病)。传统长期动物实验评估表柔比星的致癌潜力尚未进行,但静脉政府单一剂量3.6毫克/公斤盐酸表柔比星的雌性老鼠(约0.2倍人类最大推荐剂量的身体表面积的基础上)乳腺肿瘤的发病率大约翻了一番(主要是纤维肿瘤)观察到1年。政府0.5毫克/公斤盐酸表柔比星静脉注射的老鼠(约0.025倍人类最大推荐剂量的身体表面积的基础上)每3周十剂量增加皮下纤维瘤的发病率在男性超过18个月的观察期。此外,皮下管理0.75或1.0毫克/公斤/天(约0.015倍人类最大推荐剂量在身体表面面积的基础上)为4天新生大鼠出生后第一和第十天总共八个剂量增加动物肿瘤的发病率比控制在24个月的观察期。
盐酸表柔比星是诱变在体外细菌(艾姆斯测试)在代谢活化的存在与否和哺乳动物细胞(国科中国仓鼠肺成纤维细胞HGPRT试验)在缺乏而不是代谢活化的存在。盐酸表柔比星是致染色体断裂的在体外(在人类淋巴细胞染色体畸变)的存在和缺乏代谢活化和也致染色体断裂的在活的有机体内(在小鼠骨髓染色体畸变)。
在生育对老鼠的研究中,雄性有盐酸表柔比星每天9周,与雌性交配的是盐酸表柔比星每天交配前2周和怀孕的第七天。当0.3毫克/公斤/天(约0.015倍的最大推荐人类身体表面积的基础上单剂量)管理的男女,没有怀孕了。没有观察到交配行为或影响生育0.1毫克/公斤/天,但雄性大鼠睾丸和附睾萎缩,并降低精子发生。0.1毫克/公斤/天剂量也embryolethality引起的。增加这些研究观察胎儿生长迟缓的发生率为0.03毫克/公斤/天(约0.0015倍的最大推荐人类身体表面积的基础上单剂量)。多个每日剂量表阿霉素的兔子和狗也引起男性生殖器官的萎缩。单20.5和12毫克/公斤剂量的静脉注射盐酸表柔比星引起睾丸萎缩在小鼠和大鼠,分别(约0.5倍人类最大推荐剂量的身体表面积的基础上)。单剂量为16.7毫克/公斤盐酸表柔比星导致大鼠子宫萎缩。
尽管实验数据并不可用,盐酸表柔比星注射液可以引起人类精子的染色体损伤由于其基因毒性的潜力。男性接受注射用盐酸表柔比星治疗应使用有效的避孕方法。盐酸表柔比星注射液可能会导致不可逆转的闭经(过早绝经)在绝经前妇女。
消除表柔比星的主要路线是肝胆的系统(见临床药理学,药物动力学在特殊人群)。血清总胆红素和AST水平应该评价注射用盐酸表柔比星治疗之前和期间。胆红素升高或AST患者可能经历的间隙较慢,药物总体毒性增加。低剂量建议这些病人(见剂量和管理)。对严重肝损伤患者没有评估;因此,不应使用盐酸表柔比星在这个患者人群。
血清肌酐应该评估之前和期间治疗。剂量的调整是必要的患者的血清肌酐> 5 mg / dL(见剂量和管理)。接受透析的患者没有被研究过。
与其他细胞毒性剂,盐酸表阿霉素注射可能引起高尿酸血由于伴随药物引起的广泛的嘌呤分解代谢迅速溶解高度敏感的肿瘤细胞(肿瘤溶解综合征)。还可能出现其他代谢异常。虽然不是一般在乳腺癌患者,医生应该考虑潜在的易感患者肿瘤溶解综合征的可能性和应考虑监测血清尿酸、钾、钙、磷酸和肌酸酐初始化疗后管理。水化、碱化尿液和预防与别嘌呤醇预防高尿酸血肿瘤溶解综合症的可能减少潜在的并发症。
盐酸表阿霉素注射可能导致胎儿的伤害当管理一个孕妇。管理0.8毫克/公斤/天静脉注射盐酸表柔比星的老鼠(约0.04倍的最大推荐单人类剂量在身体表面面积的基础上)在5到15天的妊娠是embryotoxic(增加吸收和post-implantation损失),导致胎儿生长迟缓(体重下降),但没有产生畸形的剂量。管理2毫克/公斤/天静脉注射盐酸表柔比星的老鼠(约0.1倍的最大推荐单人类剂量在身体表面面积的基础上)的第9和第10天妊娠embryotoxic(增加吸收,post-implantation损失,和死去的胎儿;和住胎儿下降),胎儿生长阻滞(体重下降),并造成胎盘重量下降。这种剂量也产生畸形的,引起众多外部(肛门闭锁,畸形的尾巴,异常生殖结节),内脏(主要是胃肠道、泌尿系统和心血管系统),和骨骼(变形长骨骼和腰带,肋骨异常,不规则的脊髓骨化)畸形。管理静脉注射盐酸表柔比星兔子在剂量高达0.2毫克/公斤/天(约0.02倍的最大推荐单人类剂量在身体表面面积的基础上)在6到18天的妊娠并非embryotoxic或畸形形成的,而是一个母亲般地有毒剂量的0.32毫克/公斤/天增加堕胎和骨化延迟。管理的母体毒性的静脉注射剂量的1毫克/公斤/天表柔比星兔子(约0.1倍最大推荐单人类剂量在身体表面面积的基础上)天10到12的妊娠人工流产,但没有其他的迹象embryofetal毒性或致畸性。当剂量为0.5毫克/公斤/天表阿霉素注射大鼠从17天交货后21天的妊娠(约0.025倍的最大推荐单人类剂量在身体表面面积的基础上),没有永久的改变中观察到开发、功能活动,行为,或后代的繁殖性能。
没有足够的,在孕妇的、严谨的研究报告。两个怀孕已报告在服用盐酸表柔比星的女性。一个34岁的女人,怀孕28周在乳腺癌的诊断、治疗与环磷酰胺和表柔比星每3周3周期。她收到了最后剂量在怀孕34周和交付一个健康的婴儿在35周。一个34岁的女人与乳腺癌转移到肝脏随机FEC-50但因为怀孕被撤的研究。她经历了一次自然流产。如果在怀孕期间使用盐酸表柔比星,或者病人怀孕时服用这种药物,病人应该通知对胎儿的潜在危害。妇女的生育潜力应该建议避免怀孕。
法律问题
目前还没有法律信息用于这种药物。
FDA安全警报
目前没有FDA安全警告这种药物。
制造商警告
目前还没有这种药物制造商警告信息。
FDA标记变化
目前没有FDA标签更改用于这种药物。
使用
盐酸表柔比星注射液表示作为辅助治疗的一个组成部分患者腋窝的证据节点肿瘤切除后参与原发性乳腺癌。
历史
目前还没有药物可用于这种药历史。
其他信息
盐酸表柔比星注射液是一种蒽环霉素细胞毒性剂,用于静脉管理。盐酸表柔比星注射液无菌,提供清晰、红色溶液,可在玻璃小瓶含有50和200毫克盐酸表柔比星不含防腐剂,现成的解决方案。每毫升溶液包含2毫克盐酸表柔比星。活性成分包括氯化钠、USP和注射用水,早餐。溶液的pH值调整到3.0了盐酸、NF。
盐酸表柔比星是4-epimer阿霉素和柔毛霉素的半合成衍生物。化学名称(s - 8日独联体)-10 - ((3-amino-2 3 6-trideoxy-α-L -arabino-hexopyranosyl)氧]7,8,9,10 - tetrahydro6, 8日11-trihydroxy-8——(hydroxyacetyl) 1-methoxy-5 12-naphthacenedione盐酸。活性成分是红橙色吸湿粉、实验式C27H29日没有11盐酸和分子量为579.95。结构式如下:
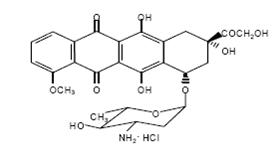
NH2∙盐酸
来源
盐酸表柔比星制造商
-
Generamedix公司。

盐酸表柔比星| Generamedix公司。
![Epirubicin Hydrochloride (Epirubicin Hydrochloride) Injection, Solution [Generamedix, Inc.] 盐酸表柔比星(盐酸表柔比星)注射,解决方案(Generamedix, Inc .)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
盐酸表柔比星注射液是由静脉输液管理病人。盐酸表柔比星注射液在反复3 - 4周周期。盐酸表柔比星的总剂量注射可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星注射液的推荐剂量如下:
起始剂量盐酸表柔比星注射液的推荐起始剂量是100到120 mg / m2。以下方案中使用了试验支持使用盐酸表柔比星注射液辅助治疗的一个组成部分患者腋下淋巴结阳性乳腺癌:
cef - 120:
环磷酰胺75 mg / m2阿宝D 1 - 14所示
盐酸表柔比星注射液60 mg / m2 IV D 1, 8
5 -氟尿嘧啶500 mg / m2 4 D 1, 8
重复每28天6周期
选举委员会- 100:
5 -氟尿嘧啶500毫克/平方米
盐酸表柔比星注射液100毫克/平方米
环磷酰胺500毫克/平方米
第一天所有药物进行静脉注射,每21天重复6周期
病人服用120 mg / m2的盐酸表阿霉素注射甲氧苄氨嘧啶也接受预防性抗生素治疗(例如,Septra®Bactrim™)或氟喹诺酮类。
*光谱®是君主药品的注册商标,公司。
基于“增大化现实”技术的科学* Bactrim™是一个商标。
骨髓功能障碍管理应该考虑低起始剂量(75 - 90 mg / m2)严重预防患者,患者的骨髓抑郁,或肿瘤骨髓浸润的存在(见警告和预防措施)。
肝脏功能障碍明确的建议关于肝脏功能障碍患者使用盐酸表柔比星注射液不可用,因为肝功能异常患者被排除参与选举委员会的辅助试验- 100 / cef - 120治疗。患者的血清AST升高或血清总胆红素浓度,剂量减少后被推荐在临床试验中,尽管一些经验丰富的肝损伤患者:
胆红素1.2到3 mg / dL或AST 2到4次正常的1/2推荐起始剂量的上限
胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限
信息经验,肝脏功能障碍患者提供临床药理学,药物动力学在特殊人群。
肾脏功能障碍虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,低剂量应考虑患者的严重肾功能损害(血清肌酐> 5 mg / dL)。
剂量的修改剂量调整后第一个治疗周期应根据血液和nonhematologic毒性。患者治疗周期中经历低谷血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3或4 nonhematologic毒性应该在后续周期第一天剂量减少到75%的第一天剂量在当前周期。第一天化疗治疗在后续课程应该推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。病人接受一个分裂剂盐酸表柔比星注射液(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000到100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3,或3或4级nonhematologic毒性发生,第八天剂量应省略。
准备和管理措施注射用药物的药物产品应检查视觉颗粒物和变色政府之前,每当解决方案和容器许可证。程序通常用于妥善处理和处置的抗癌药物应考虑使用盐酸表阿霉素注射。在这个问题上一直beplay体验发表一些指导方针。1到8
保护措施应采取以下保护措施在处理盐酸表柔比星注射液:
人员应培训在适当的调整和处理的技术。
怀孕员工应被排除在使用这种药物。
人员处理盐酸表柔比星注射液应穿防护服:护目镜,礼服和一次性手套和口罩。
指定区域应该被定义为注射器准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。
用于重建,所有项目管理或清洁(包括手套)应放置在高风险、高温焚烧废物处理袋。
溢出或泄漏应该处理稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。所有污染和清洁材料应放置在高风险、焚烧废物处理袋。偶然接触皮肤或眼睛应立即治疗通过丰富的灌洗水,肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。应该寻求医疗救助。总是在脱手套后洗手。
不兼容长期接触碱性pH值的任何解决方案都应避免,因为它会导致药物的水解。盐酸表柔比星注射液不应与肝素或混合氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星注射液可用于与其他抗肿瘤药物组合,但它不推荐与其他药物混合在同一注射器。
浸出溶液的制备盐酸表柔比星注射液不含防腐剂,提供现成的解决方案。
盐酸表柔比星注射液应的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120毫克/ m2should通常有盐酸表柔比星注入超过15到20分钟。病人需要低剂量表阿霉素开始由于器官功能障碍或需要修改的剂量表阿霉素治疗期间,表阿霉素灌注时间可能是按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见注意事项)。盐酸表柔比星注射液应该在24小时内使用的第一橡胶塞的渗透。丢弃任何未使用的解决方案。
-
Otn仿制药公司。

盐酸表柔比星| Otn仿制药公司。
![Epirubicin Hydrochloride (Epirubicin Hydrochloride ) Injection, Solution [Otn Generics Inc.] 盐酸表柔比星(盐酸表柔比星)注射,解决方案(Otn仿制药公司。)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
盐酸表柔比星注射液是由静脉输液管理病人。盐酸表柔比星在反复3 - 4周周期。盐酸表柔比星的总剂量注射可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星的推荐剂量如下:
起始剂量盐酸表柔比星的推荐起始剂量是100到120 mg / m2。以下方案中使用了试验支持使用盐酸表柔比星的一个组成部分,在腋下淋巴结阳性乳腺癌患者辅助治疗:
cef - 120:环磷酰胺
盐酸表柔比星
5 -氟尿嘧啶
重复每28天6周期75 mg / m2阿宝D 1 - 14
60 mg / m2 IV D 1, 8
500毫克/平方米4 D 1 8选举委员会- 100:5 -氟尿嘧啶
盐酸表柔比星
环磷酰胺500毫克/平方米
100毫克/平方米
500 mg / m2所有药物管理第一天静脉注射,每21天重复6周期病人服用120 mg / m2的盐酸表柔比星甲氧苄氨嘧啶也接受预防性抗生素治疗(例如,Septra®, Bactrim®)或氟喹诺酮类。
骨髓功能障碍管理应该考虑低起始剂量(75 - 90 mg / m2)严重患者预处理,预先存在的骨髓抑郁症患者或肿瘤骨髓浸润的存在(见警告和预防措施)。
肝脏功能障碍明确的建议关于肝脏功能障碍患者使用盐酸表柔比星没有因为肝功能异常患者被排除在参与选举委员会的辅助试验- 100 / cef - 120治疗。患者的血清AST升高或血清总胆红素浓度,剂量减少后被推荐在临床试验中,尽管一些经验丰富的肝损伤患者:
胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限信息经验,肝脏功能障碍患者提供临床药理学,药物动力学在特殊人群。
肾脏功能障碍虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,低剂量应考虑患者的严重肾功能损害(血清肌酐> 5 mg / dL)。
剂量的修改剂量调整后第一个治疗周期应根据血液和nonhematologic毒性。患者治疗周期中经历低谷血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性应该在后续周期第一天剂量减少到75%的第一天剂量在当前周期。第一天化疗治疗在后续课程应该推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
病人接受一个分裂的剂量表阿霉素(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000 - 100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3 3/4级nonhematologic毒性发生,第八天剂量应省略。
准备和管理措施注射用药物的药物产品应检查视觉颗粒物和变色政府之前,每当解决方案和容器许可证。程序通常用于适当的处理和处置与表阿霉素抗癌药物应该考虑使用。在这个问题上一直beplay体验published.1-8一些指导方针
保护措施应采取以下保护措施在处理盐酸表柔比星:
人员应培训在适当的调整和处理的技术。怀孕员工应被排除在使用这种药物。人员处理盐酸表柔比星应该穿防护服:护目镜,礼服和一次性手套和口罩。指定区域应该被定义为注射器准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。用于重建,所有项目管理或清洁(包括手套)应放置在高风险、高温焚烧废物处理袋。溢出或泄漏应该处理稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。所有污染和清洁材料应放置在高风险、焚烧废物处理袋。偶然接触皮肤或眼睛应立即治疗通过丰富的灌洗水,肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。应该寻求医疗救助。 Always wash hands after removing gloves. Incompatibilities长期接触碱性pH值的任何解决方案都应避免,因为它会导致药物的水解。盐酸表柔比星不应与肝素或混合氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星可以与其他抗肿瘤药物结合使用,但它不是建议应与其他药物混合在同一注射器。
浸出溶液的制备盐酸表柔比星提供不含防腐剂,现成的解决方案。
盐酸表柔比星的油管应自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该表柔比星注入超过15 - 20分钟。病人需要低剂量表阿霉素开始由于器官功能障碍或需要修改的剂量表阿霉素治疗期间,表阿霉素灌注时间可能是按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见注意事项)。盐酸表柔比星应该在24小时内使用的橡胶塞的渗透。丢弃任何未使用的解决方案。
-
应用药物,有限责任公司

盐酸表柔比星|应用制药有限责任公司
![Epirubicin Hydrochloride Injection, Solution [App Pharmaceuticals, Llc] 盐酸表柔比星注射液、解决方案(应用药物,Llc)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
盐酸表柔比星注射液是由静脉输液管理病人。盐酸表柔比星注射液在重复3 - 4周周期。盐酸表柔比星的总剂量可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星的推荐剂量如下:
起始剂量
的推荐起始剂量表阿霉素hyrochloride注入是100到120毫克/米2。以下方案被用于试验支持使用盐酸表柔比星hyrochloride注入的组件在腋下淋巴结阳性乳腺癌患者辅助治疗:
cef - 120:
环磷酰胺
75 mg / m2阿宝D 1 - 14所示
盐酸表柔比星
60 mg / m2输液D 1, 8
5 -氟尿嘧啶
500 mg / m2输液D 1, 8
重复每28天6周期
选举委员会- 100:
5 -氟尿嘧啶
500毫克/平方米
盐酸表柔比星
100毫克/平方米
环磷酰胺
500毫克/平方米
第一天所有药物进行静脉注射,每21天重复6周期
病人服用120毫克/米2的盐酸表柔比星甲氧苄氨嘧啶也接受预防性抗生素治疗(例如,Septra®, Bactrim®)或氟喹诺酮类。骨髓功能障碍。管理应该考虑低起始剂量(75 - 90 mg / m2)严重预防患者,患者的骨髓抑郁,或肿瘤骨髓浸润的存在(见警告和预防措施部分)。
肝脏功能障碍。明确的建议关于肝脏功能障碍患者使用盐酸表柔比星没有因为肝功能异常患者被排除在参与选举委员会的辅助试验- 100 / cef - 120治疗。患者的血清AST升高或血清总胆红素浓度,剂量减少后被推荐在临床试验中,尽管一些经验丰富的肝损伤患者:
胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限信息经验,肝脏功能障碍患者提供临床药理学,药物动力学在特殊人群部分。
肾脏功能障碍。虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,低剂量应考虑患者的严重肾功能损害(血清肌酐> 5 mg / dL)。
剂量的修改
剂量调整后第一个治疗周期应根据血液和nonhematologic毒性。患者治疗周期中经历低谷血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性应该在后续周期第一天剂量减少到75%的第一天剂量在当前周期。第一天化疗治疗在后续课程应该推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
病人接受一个分裂剂盐酸表柔比星(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000到100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3 3/4级nonhematologic毒性发生,第八天剂量应省略。
准备和管理措施
注射用药物的药物产品应检查视觉颗粒物和变色政府之前,每当解决方案和容器许可证。程序通常用于妥善处理和处置的抗癌药物应考虑使用盐酸表柔比星。在这个问题上一直beplay体验published.1-8一些指导方针
保护措施。应采取以下保护措施在处理盐酸表柔比星注射液:
人员应培训在适当的调整和处理的技术。怀孕员工应被排除在使用这种药物。人员处理盐酸表柔比星应穿防护服:护目镜,礼服和一次性手套和口罩。指定区域应该被定义为注射器准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。用于重建,所有项目管理或清洁(包括手套)应放置在高风险、高温焚烧废物处理袋。溢出或泄漏应该处理稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。所有污染和清洁材料应放置在高风险、焚烧废物处理袋。偶然接触皮肤或眼睛应立即治疗通过丰富的灌洗水,肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。应该寻求医疗救助。总是在脱手套后洗手。
不兼容问题。长期接触碱性pH值的任何解决方案都应避免,因为它会导致药物的水解。盐酸表柔比星不应与肝素或混合氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星可以与其他抗肿瘤药物结合使用,但它不是建议应与其他药物混合在同一注射器。
浸出溶液的制备
盐酸表柔比星注射液不含防腐剂,提供现成的解决方案。
盐酸表柔比星注射液应的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120毫克/ m2should通常有盐酸表柔比星注入超过15到20分钟。病人需要低剂量表阿霉素开始由于器官功能障碍或需要修改的剂量表阿霉素治疗期间,表阿霉素灌注时间可能是按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(参见预防措施部分)。盐酸表柔比星注射液应该在24小时内使用的第一橡胶塞的渗透。丢弃任何未使用的解决方案。
-
绿岩,有限责任公司

盐酸表柔比星|绿岩,Llc
![Epirubicin Hydrochloride Injection, Solution [Greenstone, Llc] 盐酸表柔比星注射液、解决方案(绿岩,Llc)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
在可能的情况下,降低发展中毒性的风险接受盐酸表柔比星的病人在停止治疗后与其他cardiotoxic代理,特别是那些长半衰期如曲妥珠单抗、表柔比星HCl-based治疗应该推迟到其他代理已报关循环(见警告和注意事项(5.3))。
管理盐酸表柔比星注射液静脉输注。给盐酸表柔比星在重复3 - 4周周期。盐酸表柔比星的总剂量可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星的推荐剂量如下:
2.1推荐剂量盐酸表柔比星的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:环磷酰胺75 mg / m2阿宝D 1 - 14盐酸表柔比星60 mg / m2 IV D 1 8 5 -氟尿嘧啶500 mg / m2 IV D 1, 8重复每28天6周期选举委员会- 100:5 -氟尿嘧啶500 mg / m2盐酸表阿霉素100毫克/平方米环磷酰胺500 mg / m2所有药物管理第一天静脉注射,每21天重复6周期病人服用120 mg / m2的盐酸表柔比星应该接受预防性抗生素治疗。
2.2剂量修改盐酸表柔比星剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表柔比星第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重患者预处理,预先存在的骨髓抑郁症患者或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000 - 100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对肝损伤患者使用盐酸表柔比星没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。该稠化产品将回到稍微粘稠移动解决方案最多2到4小时后平衡控制室温(15 - 25ºC)。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星。在这个问题上一直beplay体验发表一些指导方针。1 - 4(见参考资料(15))。
保护措施
采取以下保护措施在处理盐酸表柔比星:
培训人员在适当的调整和处理的技术。排除怀孕员工使用这种药物。穿防护服:护目镜,礼服,当处理盐酸表柔比星和一次性手套和口罩。定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星与肝素或氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注入超过15 - 20分钟。病人需要低剂量盐酸表柔比星开始由于器官功能障碍或需要修改的剂量盐酸表柔比星治疗期间,盐酸表阿霉素灌注时间可能是按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。在24小时内使用盐酸表柔比星第一橡胶塞的渗透。丢弃任何未使用的解决方案。
-
阿海珐制药有限公司

盐酸表柔比星|阿海珐集团制药有限公司
![Epirubicin Hydrochloride Injection [Areva Pharmaceuticals,inc.] 盐酸表柔比星注射液(阿海珐制药有限公司)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
如果可能的话,降低发展中毒性的风险接受盐酸表柔比星的病人在停止治疗后与其他cardiotoxic代理,特别是那些长半衰期如曲妥珠单抗、表柔比星HYDROCHLORIDE-based治疗应该推迟到其他代理已报关循环(见警告和注意事项(5.3))。管理盐酸表柔比星注射液静脉输注。给盐酸表柔比星在重复3 - 4周周期。盐酸表柔比星的总剂量可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星的推荐剂量如下:
2.1推荐剂量盐酸表柔比星的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:环磷酰胺750 mg / m2阿宝D 1 - 14
盐酸表柔比星HYDROCHLROIDE 60 mg / m2 IV D 1, 8
5 -氟尿嘧啶500 mg / m2 4 D 1, 8
重复每28天6周期
选举委员会- 100:5 -氟尿嘧啶500毫克/平方米
盐酸表柔比星HYDROCHLROIDE 100毫克/平方米
Cylcophosphamide 500毫克/平方米
第一天所有药物进行静脉注射,每21天重复6周期
病人服用120 mg / m2的盐酸表柔比星应该接受预防性抗生素治疗。
2.2剂量修改盐酸表柔比星剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表柔比星第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重患者预处理,预先存在的骨髓抑郁症患者或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000 - 100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对肝损伤患者使用盐酸表柔比星没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
•胆红素1.2到3 mg / dL或AST 2到4次正常的1/2推荐起始剂量的上限
•胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限
肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。该稠化产品将回到稍微粘稠移动解决方案最多2到4小时后平衡控制室温(15 - 25ºC)。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星。在这个问题上一直beplay体验发表一些指导方针。1 - 4(见参考资料(15))。
保护措施
采取以下保护措施在处理盐酸表柔比星:培训人员在适当的调整和处理的技术。排除怀孕员工使用这种药物。穿防护服:护目镜,礼服,当处理盐酸表柔比星和一次性手套和口罩。定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星与肝素或氟尿嘧啶由于可能导致降水的化学不相容。盐酸表柔比星可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注入超过15 - 20分钟。病人需要低剂量盐酸表柔比星开始由于器官功能障碍或需要修改的剂量盐酸表柔比星治疗期间,盐酸表阿霉素灌注时间可能是按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。在24小时内使用盐酸表柔比星第一橡胶塞的渗透。丢弃任何未使用的解决方案。
-
Teva肠胃外的药品公司。

盐酸表柔比星| Teva肠胃外的药品公司。
![Epirubicin Hydrochloride Injection, Solution [Teva Parenteral Medicines, Inc.] 盐酸表柔比星注射液、解决方案(Teva静脉药物,Inc .)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
在可能的情况下,降低发展中毒性的风险病人停止治疗后接受盐酸表柔比星注射液与其它cardiotoxic代理,特别是那些长半衰期如曲妥珠单抗、盐酸表柔比星喷射治疗应该推迟到其他代理已报关循环(见警告和注意事项(5.3))。
管理盐酸表柔比星注射液静脉输注。给盐酸表柔比星针重复3到4周周期。盐酸表柔比星的总剂量注射可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星注射液的推荐剂量如下:
2.1推荐剂量盐酸表柔比星注射液的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:
环磷酰胺
75 mg / m2阿宝D 1 - 14所示
盐酸表柔比星注射液
60 mg / m2 IV D 1, 8
5 -氟尿嘧啶
500 mg / m2 4 D 1, 8
重复每28天6周期
选举委员会- 100:
5 -氟尿嘧啶
500毫克/平方米
盐酸表柔比星注射液
100毫克/平方米
环磷酰胺
500毫克/平方米
第一天所有药物进行静脉注射,每21天重复6周期
2.2剂量修改
患者服用120 mg / m2的盐酸表阿霉素注射应该接受预防性抗生素治疗。盐酸表柔比星注射液剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表阿霉素注射第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重患者,预处理既存的患者骨髓抑郁,或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星注射液(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000到100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对患者使用盐酸表柔比星注射液肝损伤没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
•胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量•胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。这稠化产品将回到稍微粘稠的移动解决方案最多2到4小时后平衡在控制房间温度(15 - 25°C)。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星注射液。一些指导方针在这beplay体验个问题上一直published1-4(参见参考资料(15))。
保护措施
采取以下保护措施在处理盐酸表柔比星注射液:
•培训人员在适当的调整和处理的技术。•排除怀孕员工使用这种药物。•穿防护服:护目镜、礼服和一次性手套和面具在处理盐酸表阿霉素注射。•定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。•把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。•治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星注射液与肝素或氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星注射液可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理注入盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注射液注入超过15到20分钟。病人需要盐酸表柔比星注射液低剂量开始由于器官功能障碍或需要修改的盐酸表阿霉素注射剂量治疗期间,盐酸表柔比星注射液输液时间可以按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。先用盐酸表阿霉素注射后24小时内渗透的橡胶塞。丢弃任何未使用的解决方案。
-
Amneal-agila,有限责任公司

盐酸表柔比星| Amneal-agila Llc
![Epirubicin Hydrochloride Injection [Amneal-agila, Llc] 盐酸表柔比星注射液(Amneal-agila, Llc)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
在可能的情况下,降低发展中毒性的风险病人停止治疗后接受盐酸表柔比星注射液与其它cardiotoxic代理,特别是那些长半衰期如曲妥珠单抗、盐酸表柔比星喷射治疗应该推迟到其他代理已报关循环(见警告和注意事项(5.3))。
管理盐酸表柔比星注射液静脉输注。给盐酸表柔比星注射液在重复3 - 4周周期。盐酸表柔比星的总剂量注射可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星注射液的推荐剂量如下:
2.1推荐剂量盐酸表柔比星注射液的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:环磷酰胺75 mg / m2阿宝D 1 - 14盐酸表阿霉素注射60 mg / m2 IV D 1 8 5 -氟尿嘧啶500 mg / D m2IV 8重复每28天6周期选举委员会- 100:5 -氟尿嘧啶500 mg / m2盐酸表柔比星注射液100 mg / m2环磷酰胺500 mg / m2所有药物管理第一天静脉注射,每21天重复6周期病人服用120 mg / m2的盐酸表阿霉素注射应该接受预防性抗生素治疗。
2.2剂量修改盐酸表柔比星注射液剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表阿霉素注射第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重预防患者,患者的骨髓抑郁,或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星注射液(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000到100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对患者使用盐酸表柔比星注射液肝损伤没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。该稠化产品将回到稍微粘稠移动解决方案最多2到4小时后平衡在控制房间温度(15º25ºC)。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星注射液。在这个问题上一直beplay体验发表一些指导方针。1 - 4(见参考资料(15))。
保护措施
采取以下保护措施在处理盐酸表柔比星注射液:
培训人员在适当的调整和处理的技术。排除怀孕员工使用这种药物。穿防护服:护目镜,礼服和一次性手套和口罩在处理盐酸表阿霉素注射。定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星注射液与肝素或氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星注射液可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理注入盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注射液注入超过15到20分钟。病人需要盐酸表柔比星注射液低剂量开始由于器官功能障碍或需要修改的盐酸表阿霉素注射剂量治疗期间,盐酸表柔比星注射液输液时间可以按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。先用盐酸表阿霉素注射后24小时内渗透的橡胶塞。丢弃任何未使用的解决方案。
-
Hospira全球公司。

盐酸表柔比星| Hospira全球公司。
![Epirubicin Hydrochloride Injection, Solution [Hospira Worldwide, Inc.] 盐酸表柔比星注射液、解决方案(全球Hospira, Inc .)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
在可能的情况下,降低发展中毒性的风险病人停止治疗后接受盐酸表柔比星注射液与其它cardiotoxic代理,特别是那些长半衰期如曲妥珠单抗、盐酸表柔比星喷射治疗应该推迟到其他代理已报关循环(见警告和注意事项(5.3))。
管理盐酸表柔比星注射液静脉输注。给盐酸表柔比星注射液在重复3 - 4周周期。盐酸表柔比星的总剂量注射可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星注射液的推荐剂量如下:
2.1推荐剂量盐酸表柔比星注射液的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:
环磷酰胺
75 mg / m2阿宝D 1 - 14
盐酸表柔比星注射液
60 mg / m2 IV D 1, 8
5 -氟尿嘧啶
500 mg / m2 4 D 1, 8
重复每28天6周期
选举委员会- 100:
5 -氟尿嘧啶
500毫克/平方米
盐酸表柔比星注射液
100毫克/平方米
环磷酰胺
500毫克/平方米
第一天所有药物进行静脉注射,每21天重复6周期
病人服用120 mg / m2的盐酸表阿霉素注射应该接受预防性抗生素治疗。
2.2剂量修改盐酸表柔比星注射液剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表阿霉素注射第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重患者预处理,预先存在的骨髓抑郁症患者或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星注射液(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000 - 100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对患者使用盐酸表柔比星注射液肝损伤没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
•胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量•胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。该稠化产品将回到稍微粘稠移动解决方案最多2到4小时后平衡在室温(15 - 25°C)控制。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星注射液。在这个问题上一直beplay体验发表一些指导方针。1 - 4(15)(参见参考资料。)
保护措施
采取以下保护措施在处理盐酸表柔比星注射液:
•培训人员在适当的调整和处理的技术。•排除怀孕员工使用这种药物。•穿防护服:护目镜、礼服和一次性手套和面具在处理盐酸表阿霉素注射。•定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。•把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。•治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星注射液与肝素或氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星注射液可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理注入盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注射液注入超过15 - 20分钟。病人需要盐酸表柔比星注射液低剂量开始由于器官功能障碍或需要修改的盐酸表阿霉素注射剂量治疗期间,盐酸表柔比星注射液输液时间可以按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。先用盐酸表阿霉素注射后24小时内渗透的橡胶塞。丢弃任何未使用的解决方案。
2.1推荐剂量盐酸表柔比星注射液的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:
环磷酰胺
75 mg / m2阿宝D 1 - 14
盐酸表柔比星注射液
60 mg / m2 IV D 1, 8
5 -氟尿嘧啶
500 mg / m2 4 D 1, 8
重复每28天6周期
选举委员会- 100:
5 -氟尿嘧啶
500毫克/平方米
盐酸表柔比星注射液
100毫克/平方米
环磷酰胺
500毫克/平方米
第一天所有药物进行静脉注射,每21天重复6周期
病人服用120 mg / m2的盐酸表阿霉素注射应该接受预防性抗生素治疗。
2.2剂量修改盐酸表柔比星注射液剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表阿霉素注射第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重患者预处理,预先存在的骨髓抑郁症患者或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星注射液(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000 - 100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对患者使用盐酸表柔比星注射液肝损伤没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
•胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量•胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。该稠化产品将回到稍微粘稠移动解决方案最多2到4小时后平衡在室温(15 - 25°C)控制。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星注射液。在这个问题上一直beplay体验发表一些指导方针。1 - 4(15)(参见参考资料。)
保护措施
采取以下保护措施在处理盐酸表柔比星注射液:
•培训人员在适当的调整和处理的技术。•排除怀孕员工使用这种药物。•穿防护服:护目镜、礼服和一次性手套和面具在处理盐酸表阿霉素注射。•定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。•把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。•治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星注射液与肝素或氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星注射液可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理注入盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注射液注入超过15 - 20分钟。病人需要盐酸表柔比星注射液低剂量开始由于器官功能障碍或需要修改的盐酸表阿霉素注射剂量治疗期间,盐酸表柔比星注射液输液时间可以按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。先用盐酸表阿霉素注射后24小时内渗透的橡胶塞。丢弃任何未使用的解决方案。
-
山德士公司

盐酸表柔比星|山德士公司的
![Epirubicin Hydrochloride Injection, Solution [Sandoz Inc] 盐酸表柔比星注射液、解决方案(Sandoz Inc .)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
在可能的情况下,降低发展中毒性的风险病人停止治疗后接受盐酸表柔比星注射液与其它cardiotoxic代理,特别是那些长半衰期如曲妥珠单抗、盐酸表柔比星喷射治疗应该推迟到其他代理已报关循环(见警告和注意事项(5.3))。管理盐酸表柔比星注射液静脉输注。给盐酸表柔比星注射液在重复3 - 4周周期。盐酸表柔比星的总剂量注射可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星注射液的推荐剂量如下:
2.1推荐剂量盐酸表柔比星注射液的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:
环磷酰胺
75 mg / m2阿宝D 1 - 14所示
盐酸表柔比星注射液
60 mg / m2 IV D 1, 8
5 -氟尿嘧啶
500 mg / m2 4 D 1, 8
重复每28天6周期
选举委员会- 100:
5 -氟尿嘧啶
500毫克/平方米
盐酸表柔比星注射液
100毫克/平方米
环磷酰胺
500毫克/平方米
第一天所有药物进行静脉注射,每21天重复6周期
病人服用120 mg / m2的盐酸表阿霉素注射应该接受预防性抗生素治疗。
2.2剂量修改盐酸表柔比星注射液剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表阿霉素注射第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重预防患者,患者的骨髓抑郁,或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星注射液(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000到100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对患者使用盐酸表柔比星注射液肝损伤没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
•胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量•胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。这稠化产品将回到稍微粘稠的移动解决方案最多2到4小时后平衡在控制房间温度(15到25ºC)。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星注射液。在这个问题上一直beplay体验发表一些指导方针。1 - 4(见参考资料(15))。
保护措施
采取以下保护措施在处理盐酸表柔比星注射液:
•培训人员在适当的调整和处理的技术。•排除怀孕员工使用这种药物。•穿防护服:护目镜、礼服和一次性手套和面具在处理盐酸表阿霉素注射。•定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。•把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。•治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星注射液与肝素或氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星注射液可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理注入盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注射液注入超过15到20分钟。病人需要盐酸表柔比星注射液低剂量开始由于器官功能障碍或需要修改的盐酸表阿霉素注射剂量治疗期间,盐酸表柔比星注射液输液时间可以按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。先用盐酸表阿霉素注射后24小时内渗透的橡胶塞。丢弃任何未使用的解决方案。
-
Mylan机构有限公司

盐酸表柔比星| Mylan机构有限责任公司
![Epirubicin Hydrochloride Injection [Mylan Institutional Llc ] 盐酸表柔比星注射液(Mylan机构有限责任公司)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
在可能的情况下,降低发展中毒性的风险病人停止治疗后接受盐酸表柔比星注射液与其它cardiotoxic代理,特别是那些长半衰期如曲妥珠单抗、盐酸表柔比星注射液的治疗应该推迟到其他代理已报关循环(见警告和注意事项(5.3))。
管理盐酸表柔比星注射液静脉输注。给盐酸表柔比星注射液在重复3 - 4周周期。盐酸表柔比星的总剂量注射可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星注射液的推荐剂量如下:
2.1推荐剂量盐酸表柔比星注射液的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:
环磷酰胺
75 mg / m2阿宝D 1 - 14
盐酸表柔比星注射液
60 mg / m2 IV D 1, 8
5 -氟尿嘧啶
500 mg / m2 4 D 1, 8
重复每28天6周期
选举委员会- 100:
5 -氟尿嘧啶
500毫克/平方米
盐酸表柔比星注射液
100毫克/平方米
环磷酰胺
500毫克/平方米
第一天所有药物进行静脉注射,每21天重复6周期
病人服用120 mg / m2的盐酸表阿霉素注射应该接受预防性抗生素治疗。
2.2剂量修改盐酸表柔比星注射液剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表阿霉素注射第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重患者预处理,预先存在的骨髓抑郁症患者或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星注射液(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000 - 100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对患者使用盐酸表柔比星注射液肝损伤没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。该稠化产品将回到稍微粘稠移动解决方案最多2到4小时后平衡在控制房间温度(15°25°C)。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星注射液。在这个问题上一直beplay体验发表一些指导方针。1 - 4(见参考资料(15))。
保护措施
采取以下保护措施在处理盐酸表柔比星注射液:
培训人员在适当的调整和处理的技术。排除怀孕员工使用这种药物。穿防护服:护目镜、礼服和一次性手套和面具在处理盐酸表阿霉素注射。定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星注射液与肝素或氟尿嘧啶由于可能导致降水的化学不相容。
盐酸表柔比星注射液可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理注入盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注射液注入超过15到20分钟。病人需要盐酸表柔比星注射液低剂量开始由于器官功能障碍或需要修改的盐酸表阿霉素注射剂量治疗期间,盐酸表柔比星注射液输液时间可以按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。先用盐酸表阿霉素注射后24小时内渗透的橡胶塞。丢弃任何未使用的解决方案。
-
Sagent制药

盐酸表柔比星| Sagent药品
![Epirubicin Hydrochloride Injection [Sagent Pharmaceuticals] 盐酸表柔比星注射液(Sagent制药)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
在可能的情况下,降低发展中毒性的风险病人停止治疗后接受盐酸表柔比星注射液与其它cardiotoxic代理,特别是那些长半衰期如曲妥珠单抗、盐酸表柔比星喷射治疗应该推迟到其他代理已报关循环(见警告和注意事项(5.3))。
管理盐酸表柔比星注射液静脉输注。给盐酸表柔比星注射液在重复3 - 4周周期。盐酸表柔比星的总剂量注射可以在每个周期的第一天或平均分割,每个周期的天给1和8。盐酸表柔比星注射液的推荐剂量如下:
2.1推荐剂量盐酸表柔比星注射液的推荐剂量是100到120 mg / m2。推荐以下方案:
cef - 120:环磷酰胺
盐酸表柔比星注射液
5 -氟尿嘧啶
重复每28天6周期75 mg / m2阿宝D 1 - 14
60 mg / m2 IV D 1, 8
500 mg / m2 4 D 1, 8
选举委员会- 100:5 -氟尿嘧啶
盐酸表柔比星注射液
环磷酰胺500毫克/平方米
100毫克/平方米
500毫克/平方米第一天所有药物进行静脉注射,每21天重复6周期
病人服用120 mg / m2的盐酸表阿霉素注射应该接受预防性抗生素治疗。
2.2剂量修改盐酸表柔比星注射液剂量调整周期内的血液和non-hematologic毒性治疗,是基于最低点血小板计数< 50000 / mm3绝对中性粒细胞计数(ANC) < 250 / mm3,粒细胞减少性发热,或成绩3/4 nonhematologic毒性。减少盐酸表阿霉素注射第一天剂量在随后的周期第一天剂量的75%在当前周期。第一天化疗治疗在随后的课程推迟到血小板计数≥100000 / mm3 ANC≥1500 / mm3, nonhematologic毒性已经恢复到≤1级。
骨髓功能障碍
开始考虑管理较低剂量(75 - 90 mg / m2)严重患者预处理,预先存在的骨髓抑郁症患者或肿瘤骨髓浸润的存在(见警告和注意事项(5))。病人接受一个分裂剂盐酸表柔比星注射液(每天1和8),第八天剂量应该是75%的第一天如果血小板计数是75000 - 100000 / mm3 1000到1499 / mm3 ANC。如果一天8血小板计数< 75000 / mm3 ANC < 1000 / mm3成绩3/4 nonhematologic毒性发生,省略第八天剂量。
肝损伤
建议对患者使用盐酸表柔比星注射液肝损伤没有因为肝功能异常患者没有包含在辅助试验(见警告和注意事项(5.5)和临床药理学(12.3)]。患者的血清AST升高或血清总胆红素浓度,剂量减少建议如下:
胆红素1.2到3 mg / dL或AST 2到4次正常上限的1/2推荐起始剂量胆红素> 3 mg / dL或AST > 4次正常推荐起始剂量的1/4的上限肾功能损害
虽然没有具体的推荐剂量可以根据肾功能损害患者可用数据有限,考虑在严重肾功能损害患者低剂量(血清肌酐> 5 mg / dL)(见警告和注意事项(5.6)和临床药理学(12.3)]。
2.3准备和管理措施存储解决方案的注入在冷藏条件下会导致形成稠化产品。该稠化产品将回到稍微粘稠移动解决方案最多2到4小时后平衡控制室温(15 - 25ºC)。
检查肠胃外的药物产品视觉颗粒物和变色政府之前,每当解决方案和容器许可证。妥善处理和处置程序时应该使用抗癌药物处理和准备盐酸表柔比星注射液。在这个问题上一直beplay体验发表一些指导方针。1 - 4(见参考资料(15))。
保护措施
采取以下保护措施在处理盐酸表柔比星注射液:
培训人员在适当的调整和处理的技术。排除怀孕员工使用这种药物。穿防护服:护目镜、礼服和一次性手套和面具在处理盐酸表阿霉素注射。定义一个指定区域注射器的准备(最好是在层流系统),与工作表面受到可支配的保护,plastic-backed,吸水纸。把所有物品用于调整、管理或清洁(包括手套)高风险、高温焚烧废物处理袋。治疗溢出或泄漏与稀释次氯酸钠(1%可用氯)的解决方案,最好是泡,然后水。把所有污染和清洁材料在高风险、焚烧废物处理袋。治疗意外接触皮肤或眼睛立即通过丰富的灌洗水、肥皂和水或碳酸氢钠溶液。然而,不擦伤皮肤使用硬毛刷。寻求医疗关注。 Always wash hands after removing gloves.不兼容
避免长时间接触任何解决方案的碱性pH值,因为它会导致药物的水解。不要将盐酸表柔比星注射液与肝素或氟尿嘧啶由于可能导致降水的化学不相容。盐酸表柔比星注射液可以与其他抗肿瘤药物结合使用,但不与其他药物混合在同一注射器。
浸出溶液的制备
管理注入盐酸表柔比星的油管自由流动的静脉输液(0.9%氯化钠或5%葡萄糖溶液)。推荐起始剂量的患者接受初步治疗100 - 120 mg / m2通常应该盐酸表柔比星注射液注入超过15 - 20分钟。病人需要盐酸表柔比星注射液低剂量开始由于器官功能障碍或需要修改的盐酸表阿霉素注射剂量治疗期间,盐酸表柔比星注射液输液时间可以按比例减少,但不应少于3分钟。这种技术是为了减少血栓形成或perivenous外渗的风险,这可能导致严重的蜂窝组织炎,发泡、或组织坏死。不推荐直接推动注射由于外渗的风险,甚至可能发生在足够的血液在针吸回来。从注入静脉硬化可能导致小血管或重复注入同样(见警告和注意事项(5.9))。先用盐酸表阿霉素注射后24小时内渗透的橡胶塞。丢弃任何未使用的解决方案。
登录到你的免费帐户