FDA警告——记录显示这种药已经被召回。
| 产品描述: | 注射头孢吡肟对USP和葡萄糖注入USP, 1 g在双工,50毫升容器,产品目录号3193 - 11,第四只使用,单剂量,无菌,Rx, B布劳恩医疗公司,欧文CA 92614 - 5895, NDC 0264-3193-11 |
|---|---|
| 状态: | 正在进行的 |
| 城市: | 欧文 |
| 状态: | CA |
| 国家: | 我们 |
| 自愿/要求: | 自愿:公司发起 |
| 最初公司通知: | 信 |
| 分布模式: | 全国范围内,波多黎各和西班牙 |
| 分类: | 课上我 |
| 产品数量: | 22248个单位 |
| 召回原因: | 的颗粒物:b·布劳恩医疗公司召回几个注射产品由于可见颗粒物中发现储备样本单位。 |
| 回忆起始日期: | 20131121 |
| 报告日期: | 20140507 |
你是医学专业吗?
盐酸头孢吡肟和葡萄糖召回
得到一个警告当一个回忆。
问题&答案
副作用和不良反应
目前还没有对该产品的警告信息。我们为不便道歉。
法律问题
目前还没有法律信息用于这种药物。
FDA安全警报
目前没有FDA安全警告这种药物。
制造商警告
目前还没有这种药物制造商警告信息。
FDA标记变化
目前没有FDA标签更改用于这种药物。
使用
减少耐药细菌的开发和维护的有效性注射用头孢吡肟USP和葡萄糖注入USP和其他抗菌药物,注射用头孢吡肟USP和葡萄糖注入USP应该只用于治疗或预防感染,被证明或强烈怀疑是由敏感细菌引起的。文化和易感性信息可用时,他们应该考虑在选择或修改抗菌治疗。没有这些数据,当地流行病学和易感性可能有助于治疗的经验选择模式。
注射用头孢吡肟USP和葡萄糖注入USP表示为肺炎(中度到重度)引起的链球菌引起的肺炎(包括与并发菌血症相关病例),铜绿假单胞菌、肺炎克雷伯菌,或肠杆菌属物种。
注射用头孢吡肟USP和葡萄糖注入表示USP作为单药治疗发热性粒细胞减少性病人的治疗经验。严重感染的高危患者(包括骨髓移植患者最近的历史,与低血压在演讲中,与一个潜在的血液恶性肿瘤,或有严重或长期嗜中性白血球减少症),抗菌单一疗法可能不合适。现有的数据不足以支持头孢吡肟单药治疗的病人的疗效(见临床研究(14.1)]。
注射用头孢吡肟USP和葡萄糖注入USP表示对简单和复杂的泌尿道感染(包括肾盂肾炎)所致大肠杆菌或肺炎克雷伯菌当感染严重,或造成的大肠杆菌、肺炎克雷伯菌,或变形杆菌轻度至中度感染时,包括病例与这些微生物与并发菌血症有关。
注射用头孢吡肟USP和葡萄糖注入USP表示中度到重度的简单的皮肤和皮肤结构感染所致金黄色葡萄球菌(仅methicillin-susceptible菌株)酿脓链球菌。
注射用头孢吡肟USP和葡萄糖注入USP表示复杂腹腔感染(用于结合甲硝哒唑)所致大肠杆菌,草绿色链球菌,铜绿假单胞菌、肺炎克雷伯菌、肠杆菌属物种,或脆弱拟杆菌(见临床研究(14.2)]。
历史
目前还没有药物可用于这种药历史。
其他信息
盐酸头孢吡肟,USP是一种半合成的广谱,对注射用头孢菌素抗生素。化学名称是1 - [[(6R7R)7 - [2 - (2-amino-4-thiazolyl) -glyoxylamido] 2-carboxy-8-oxo-5-thia-1-azabicyclo [4.2.0] oct-2-en-3-yl)甲基]1-methylpyrrolidinium氯,72- (Z)- (O-methyloxime)、monohydrochloride一水,对应于以下结构式:
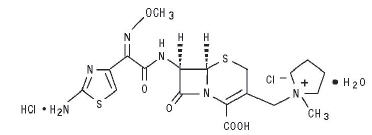
盐酸头孢吡肟(一水)的分子质量为571.50和C的分子式19H25ClN6O5年代2•HCl•H2O。
盐酸头孢吡肟是一种白色至淡黄色粉末。盐酸头孢吡肟包含相当于不少于825毫克和不超过911微克的头孢吡肟(C19H24N6O5年代2每毫克),在无水的基础上计算。它是高度溶于水。
注射用头孢吡肟USP和葡萄糖注入USP双®双室容器提供的静脉管理优势相当于1 g和2 g的头孢吡肟。注射用头孢吡肟USP和葡萄糖注入USP提供无菌,nonpyrogenic,一次性打包组合的盐酸头孢吡肟精氨酸(药品室)和50毫升的5%葡萄糖注射液(稀释剂)双®无菌容器中。
双®的粉室容器包含一个无菌、干燥的盐酸头孢吡肟和精氨酸的混合物。它包含相当于不低于90.0%,不超过115.0%的标签数量的头孢吡肟(C19H24N6O5年代2)。精氨酸,近似浓度为725毫克/克头孢吡肟,添加到控制重组方案的pH值在4.0 - 6.0。
双®容器是一个灵活的双室容器。删除可剥性箔条后,激活海豹,并彻底混合,重组药物产品是高渗的,一次性静脉注射使用。每50毫升含有盐酸头孢吡肟相当于1克或2克头孢吡肟。重组方案的注射用头孢吡肟USP和葡萄糖注入USP琥珀的颜色范围从无色。
不是用天然橡胶乳胶、PVC或Di (2-ethylhexyl)邻苯二甲酸酯(DEHP)。
双®双室容器是由一种特殊配方材料。产品(稀释剂和药物)接触层的混合热塑性橡胶和聚丙烯乙烯共聚物,不含增塑剂。容器的安全系统是由USP生物评价程序。
来源
盐酸头孢吡肟和葡萄糖制造商
-
b·布劳恩医疗公司。

盐酸头孢吡肟和葡萄糖| b·布劳恩医疗公司。
![Cefepime Hydrochloride And Dextrose (Cefepime Hydrochloride) Injection, Solution [B. Braun Medical Inc.] 盐酸头孢吡肟和葡萄糖(盐酸头孢吡肟)注射,解决方案(B。布劳恩医疗公司。)](//www.lbxkm.com/wp-content/themes/bootstrap/assets/img/loading2.gif)
2.1成人和儿科人口注射用头孢吡肟USP和葡萄糖注射USP双®容器应该使用只有在病人需要整个1或2克剂量而不是任何分数。推荐的成人和小儿剂量和管理路线表1中列出。注射用头孢吡肟USP和葡萄糖注入USP应静脉注射(IV)在大约30分钟。
表1:推荐剂量时间表注射用头孢吡肟USP和葡萄糖注入患者的USP CrCL大于60毫升/分钟*站点和类型的感染剂量频率持续时间(天)*的成年人调整剂量患者CrCL小于等于60毫升/分钟(2.2)
†包括病例与并发菌血症‡第四ForPseudomonas绿脓杆菌,使用2 g每8小时(每公斤50毫克每剂在儿科患者2个月16年)。
§或者直到解决嗜中性白血球减少症。发烧的病人解决但粒细胞减少性停留的时间超过7天,需要持续的抗菌治疗应经常重新评估。中度到重度肺炎肺炎链球菌__,铜绿假单胞菌‡,k .肺炎或肠杆菌属物种1 - 2 g IV每8 - 12小时10经验治疗发热性粒细胞减少性病人(参见适应症和用法(1)和临床研究(14)]7§2 g IV每8小时轻度至中度简单或复杂的尿路感染,如肾盂肾炎、由于大肠杆菌,肺炎,或0.5 p .奇异君子兰__每12小时1克四世7 - 10严重的简单或复杂的尿路感染,如肾盂肾炎、肺炎由于大肠杆菌或k . __第四2 g每12小时10中度到重度的简单的皮肤和皮肤结构感染由于金黄色葡萄球菌和链球菌2 g IV每12小时10复杂腹腔感染(用于结合甲硝哒唑)由大肠杆菌引起的,草绿色链球菌,铜绿假单胞菌‡,k .肺炎肠杆菌属的物种,或b . fragilis。(见临床研究(14)]2 g IV每8 - 12小时7 - 10儿科患者(2月16年)儿科患者的最大剂量不得超过推荐的成人剂量。通常的推荐剂量在儿科患者40公斤的体重对简单和复杂的泌尿道感染(包括肾盂肾炎),简单的皮肤和皮肤结构感染和肺炎是每公斤50毫克/剂量,每12小时服用(50毫克每千克每剂,每8小时对发热性粒细胞减少性病人),时间上面给出。注射用头孢吡肟USP和葡萄糖注射双®容器中的USP旨在提供1 g或2 g剂量的头孢吡肟。为了防止意外过量,此产品不应该用于儿科病人需要不到完整的成人剂量的头孢吡肟。2.2患者肾功能损害患者的肌酐清除率小于等于60毫升/分钟,注射的剂量的头孢吡肟USP和葡萄糖注入USP应调整补偿的速度较慢,肾脏消除。推荐的初始剂量的注射用头孢吡肟USP和葡萄糖注入USP应该一样在肾功能正常的患者除了接受血液透析的患者。推荐的维护剂量的注射用头孢吡肟USP和葡萄糖注入USP肾功能损害患者展示在表2。注射用头孢吡肟USP和葡萄糖注射USP双®容器应该使用只有在病人需要整个1或2克剂量而不是任何分数。
只有血清肌酐是可用的,下面的公式(科克罗夫特和Gault方程)5月1日被用来估计肌酐清除率(参见参考资料(15))。血清肌酐应该表示肾功能的稳定状态:
男性:肌酐清除率(毫升/分钟)=重量(公斤)×(140 -)72×血清肌酐(mg / dL)雌性:0.85×以上值表2:推荐剂量时间表注射用头孢吡肟USP和葡萄糖注入USP在成人患者(肾功能正常,肾功能损害和血液透析)肌酐清除率
(毫升/分钟)建议维修计划*在血液透析的日子里,注射用头孢吡肟USP和葡萄糖注入USP血液透析后应。只要有可能,注射用头孢吡肟USP和葡萄糖注入USP应每天在同一时间。大于60(常规推荐剂量计划)500毫克每12小时1 g每12小时2 g每12小时2 g每8小时30 - 60 500毫克每24小时每24小时1 g 2 g每24小时每12小时2 g 11-29 500毫克每24小时500毫克每24小时每24小时1 g 2 g每24小时不到11 250毫克每24小时250毫克每24小时500毫克每24小时每24小时1 g李500毫克每48小时1 g每48小时2 g每48小时2 g每48小时血液透析* 1 g 1天,然后每24小时500毫克每24小时之后1 g在接受连续性腹膜透析的患者,注射用头孢吡肟USP和葡萄糖注入USP通常可能在推荐剂量的剂量间隔每48小时(见表2)。
在接受血液透析的患者中,大约有68%的头孢吡肟的总量出现在身体的透析一个3小时的透析期间将被删除。剂量的注射用头孢吡肟USP和葡萄糖注入USP对血液透析患者是1克之后1天500毫克每24小时所有感染的治疗除了发热性中性粒细胞减少,也就是1 g每24小时。注射用头孢吡肟USP和葡萄糖注入USP应每天在同一时间,完成后血液透析在血液透析的日子(见表2)。
2.3准备使用注射用头孢吡肟USP和葡萄糖注射USP在双®容器中这种重组方案仅供静脉注射使用。
不要使用塑料容器串联连接。这样使用会导致空气栓塞由于残余空气从主容器之前政府的液体从二级容器就完成了。如果政府控制的泵设备,必须注意停止抽水行动在容器中运行之前干燥或空气栓塞可能的结果。
注射用药物的药物产品应检查视觉政府之前对颗粒物和变色。只使用解决方案是明确和容器和密封是否完好无损。
双®药物输送系统存储,避免无意激活,双®容器应保持在折叠的位置直到激活的目的是。病人标签和药物粉末/稀释剂检查特定的标签适用于铝箔容器。注意避免激活使用。不包括任何部分箔条的病人标签。拉开插栓边选项卡并展开双®容器(见图1)。
视觉检查稀释室内颗粒物。只使用容器和密封是否完好无损。检查药物粉末异物或变色,皮箔条从药品室(见图2)。
从光箔条后的保护。
注意:如果删除箔带,容器应re-folded边选项卡锁住,直到准备激活。产品必须在7天内使用,但不超出截止日期的标签。调整(激活)不使用后直接存储到制冷,允许产品平衡至室温在病人使用。展开双®容器和点集港口一个向下的方向。悬挂器选项卡一端开始,折叠双®容器在稀释剂半月板捕获所有空中折叠。激活,挤压折叠稀释剂室直到稀释剂之间的密封和粉打开时,将稀释剂释放到药物粉室(见图3)。
煽动水粉混合直到药物粉完全溶解。
注意:以下调整(激活),产品必须在12小时内使用存储在室温下或在5天内如果冷藏。颗粒物的政府再造的视力检查解决方案。点集港口一个向下的方向。悬挂器选项卡一端开始,折叠双®容器下方半月板捕获所有空中折叠的解决方案。挤压折叠双®之间的密封容器,直到重组药物方案和设置端口打开,释放液体设置端口(参见图4)。
附加第四集之前,检查通过挤压分钟泄漏容器坚定。如果发现泄漏,丢弃容器和解决不育可能就会大打折扣。使用无菌技术,皮箔覆盖从一组端口和连接无菌管理设置(参见图5)。
请参考附带使用说明政府。重要的政府指令集不使用串联连接。不引入添加剂双®容器。管理注射用头孢吡肟USP和静脉注射葡萄糖注射USP在大约30分钟。间歇静脉输液与一组引水系统管理可以实现兼容的解决方案。然而,在注入注射用头孢吡肟USP和葡萄糖注入USP,建议停止其他的解决方案。头孢吡肟的解决方案不应该被添加到解决方案的氨苄青霉素的浓度大于40毫克/毫升,也不应该被添加到灭滴灵、万古霉素、庆大霉素、妥布霉素、硫酸netilimicin或氨茶碱因为潜在的相互作用。然而,如果并发与头孢吡肟治疗表示,这些抗生素可以单独管理。
登录到你的免费帐户